Elektronų pasiskirstymas arba elektronų konfigūracija, kaip išdėstomi cheminiai elementai, atsižvelgiant į jų turimą elektronų skaičių ir jų artumą atomo branduoliui.
Elektroninis pakopinis paskirstymas
Po to, kai atsirado keli atominiai modeliai, Bohro modelis pasiūlė organizuoti elektrosferą į orbitas.
Elektronai yra organizuojami ir paskirstomi per elektroninius sluoksnius, vieni yra arčiau branduolio, o kiti toliau.
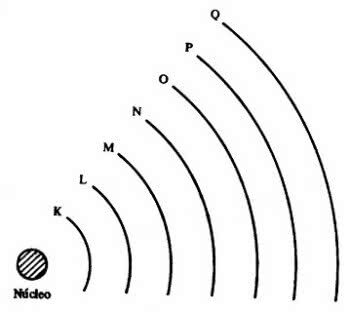
Tada atsirado 7 elektroniniai sluoksniai (K, L, M, N, O, P ir Q), kuriuos periodinėje lentelėje vaizduoja horizontalios linijos, sunumeruotos nuo 1 iki 7.
Elementai tose pačiose linijose turi tą patį didžiausią elektronų skaičių ir tą patį energijos lygį.
Taigi galima pastebėti, kad elektronai yra energijos lygiuose ir pakopose. Taigi kiekvienas turi tam tikrą energijos kiekį.
|
Energijos lygis |
Elektroninis sluoksnis |
Maksimalus elektronų skaičius |
|---|---|---|
| 1° | K. | 2 |
| 2° | L | 8 |
| 3° | M | 18 |
| 4° | N | 32 |
| 5° | O | 32 |
| 6° | P | 18 |
| 7° | Klausimas | 8 |
valentinis sluoksnis tai paskutinis elektroninis sluoksnis, tai yra išorinis atomo sluoksnis. Pagal
Aštuoneto taisyklė, atomai turi tendenciją stabilizuotis ir tapti neutralūs.Tai atsitinka, kai jie turi tą patį protonų ir neutronų kiekį, o paskutiniame elektronų apvalkale yra aštuoni elektronai.
Vėliau atsirado energijos pakopos, kurias žymi mažosios raidės s, p, d, f. Kiekvienas antrinis lygis palaiko maksimalų elektronų skaičių:
| sublygiai | Didžiausias elektronų skaičius |
|---|---|
| s | 2 |
| P | 6 |
| d | 10 |
| f | 14 |
Paulingo diagrama
Amerikiečių chemikas Linusas Carlas Paulingas (1901–1994) studijavo atomines struktūras ir sukūrė schemą, kuri naudojama iki šiol.
Paulingas rado būdą, kaip visus energijos lygius išdėstyti didėjimo tvarka, naudojant įstrižainės kryptį. Schema tapo žinoma kaip Paulingo diagrama.
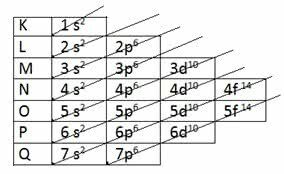
Didėjančia tvarka: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p6
Atkreipkite dėmesį, kad prieš energijos pakopą nurodytas skaičius atitinka energijos lygį.
Pavyzdžiui, per 1s2:
- s nurodo energijos pakopą
- 1 nurodo pirmąjį lygį, esantį K sluoksnyje
- 2 rodiklis nurodo elektronų skaičių šiame pakopoje
Kaip atlikti elektroninį platinimą?
Norėdami geriau suprasti elektroninio platinimo procesą, peržiūrėkite toliau pateiktą išspręstą pratimą.
1. Elektroniškai paskirstykite elementą Geležis (Fe), kurio atomo numeris 26 (Z = 26):
Taikant Linuso Paulingo diagramą, įstrižainės kertamos modeliu nurodyta kryptimi. Energijos pakopos užpildomos maksimaliu elektronų skaičiumi viename elektronų apvalkale, kol baigiasi 26 elemento elementai.
Norėdami pasiskirstyti, atkreipkite dėmesį į bendrą elektronų skaičių kiekviename pakopoje ir atitinkamuose elektroniniuose sluoksniuose:
K - s2
L - 2s2 2p6
M - 3s2 3p6 3d10
N - 4s2
Atkreipkite dėmesį, kad elektroninio paskirstymo atlikti visuose sluoksniuose nebuvo būtina, nes geležies atominis skaičius yra 26.
Taigi šio elemento elektroninis platinimas vaizduojamas taip: 1s2 2s2 2p6 3s2 3p6 4s2 3d6. Eksponentų skaičių suma yra 26, tai yra bendras geležies atome esančių elektronų skaičius.
Jei elektroninis paskirstymas nurodomas sluoksniais, jis vaizduojamas taip: K = 2; L = 8; M = 14; N = 2.
Pasinaudokite proga išbandyti savo žinias Elektroninio platinimo pratybos.
At Periodinė elementų lentelė, tai parodyta taip:

Taip pat skaitykite:
- Elektroninis bendrumas
- Kvantiniai skaičiai
- Periodinės lentelės pratimai
- Periodinės lentelės organizavimo pratimai


