Sp tipo anglies hibridizacija2 jis atsiranda, kai jis turi dvigubą jungtį ir dvi viengubas jungtis arba pi jungtį (π) ir tris sigmos jungtis (σ). Tiesą sakant, sp hibridizacija2 jis atsiranda tarp atomus, kurie užmezga dvigubą ryšį.
Tokios molekulės pavyzdys yra formaldehidas (CH2O). Atkreipkite dėmesį į jo struktūrą žemiau:
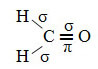
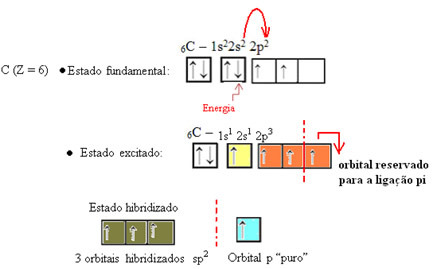
Kaip matyti tekste "sp tipo hibridizacija3“, Anglies hibridizacija įvyksta, kai elektronas iš 2 pakopos gauna energiją ir yra„ transportuojamas “į 2p sublygis ir todėl iš hibridizuotų 4 orbitalių yra kilę iš atominių orbitalių „mišinio“ grynas.
Formaldehido atveju mes žinome, kad bus pi jungtis, todėl viena iš šių hibridizuotų orbitalių yra skirta šiai jungčiai, o kitos trys atlieka sigmos ryšius:
Vandenilio atomai, kurie užmezga viengubą jungtį su anglimi, sudaro orbitą:
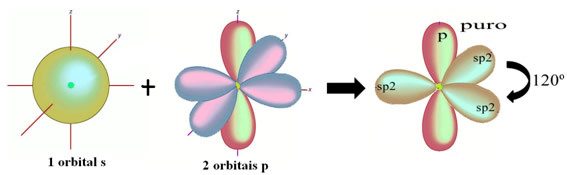
Likusi „gryna“ p orbita dvigubai sujungia deguonies atomą ir formaldehido molekulę turi tokią struktūrą:
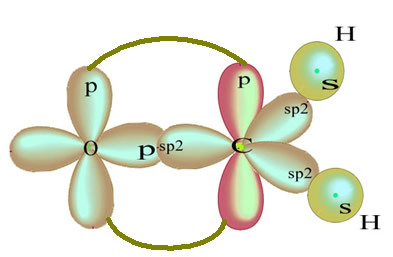
Kalbant apie šioje formaldehido struktūroje esančių obligacijų tipą, mes turime:

Jungtys: 1 = 2 = σs-sp2
3 = σp-sp2
4 =πp-p
Jennifer Fogaça
Baigė chemiją
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp2.htm
