Paulingo diagrama, taip pat žinoma kaip energijos diagrama, yra atstovavimas elektroniniam paskirstymui per energijos pakopas.
Pagal šią schemą chemikas Linusas Carlas Paulingas (1901–1994) pasiūlė tai, kas jau buvo žinoma dėl elektronų pasiskirstymo iš cheminių elementų atomų.
Norėdami pagerinti nuotaiką, Paulingas pasiūlė energijos porūšius. Per juos būtų galima išdėstyti elektronus nuo žemiausio iki aukščiausio atomo energijos lygio jo pagrindinėje būsenoje.
Elektroninis platinimas Linus Pauling
Pagal Paulingo pasiūlytą modelį elektrosfera yra padalinta į 7 elektroniniai sluoksniai (K, L, M, N, O, P ir Q) aplink atomo branduolį, kurių kiekvienas leidžia maksimalų elektronų skaičių, atitinkamai 2, 8, 18, 32, 32,18 ir 8.
At elektronikos platinimas energijos sublygiai, rodantis mažiausios energijos elektroną pirmiausia, kol pasiekia didžiausios energijos elektroną.
| Elektroniniai sluoksniai | Maksimalus elektronų skaičius | Energijos pakopos | ||||
|---|---|---|---|---|---|---|
| 1 | K. | 2 ir- | 1s2 | |||
| 2 | L | 8 ir- | 2s2 | 2p6 | ||
| 3 | M | 18 ir- | 3s2 | 3p6 | 3d10 | |
| 4 | N | 32 ir- | 4s2 | 4p6 | 4d10 | 4f14 |
| 5 | O | 32 ir- | 5s2 | 5p6 | 5d10 | 5f14 |
| 6 | P | 18 ir- | 6s2 | 6p6 | 6d10 | |
| 7 | Klausimas | 8 ir- | 7s2 | 7p6 |
K sluoksnis turi tik vieną (-ius) pakopą (-us), sluoksnis L turi du pakopas (-us ir p), sluoksnis m turi tris pakopas (-us, p ir d) ir taip.
S pakopos leidžia iki 2 elektronų, o p pakopos - iki 6 elektronų. Toliau d pakopos leidžia iki 10 elektronų, o f pakopos - iki 14 elektronų.
Atkreipkite dėmesį, kad kiekviename elektronų apvalkalo lygmenyje elgiasi elektronai, todėl kiekvienoje iš 7 apvalkalų yra didžiausias elektronų skaičius.
K: s2 = 2
L ir Q: s2 + p6 = 8
M ir P: s2 + p6 + d10 = 18
N ir O: y2 + p6 + d10 + f14= 32
Tada Paulingas atrado didėjanti energijos tvarka:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6 6s2 4f14 5d10 6p6 7s2 5f14 6d10 7p6
Diagramoje rodomos įstrižainės rodyklės, kad elementai būtų paskirstyti elektroniniu būdu:
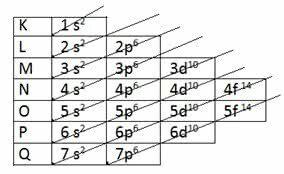 Paulingo diagrama
Paulingo diagrama
Elektroninio fosforo paskirstymo pavyzdys 15P:
1s2 2s2 2p6 3s2 3p3
patinka iki 3 metų2 iš viso jau turėjome 12 elektronų (2 + 2 + 6 + 2), mums reikia tik dar 3 elektronų iš 3p pakopos6.
Taigi galime gauti reikiamą elektronų kiekį, jei jis yra ne didesnis kaip 6, tai yra didžiausias skaičius, kurį 3p pakopoje6 elgiasi.
Skaityk ir tu Valensijos sluoksnis ir Kvantiniai skaičiai.
Išspręstos elektroninio platinimo pratybos
Klausimas 1
(„Unirio“) „Dantų implantai yra saugesni Brazilijoje ir jau atitinka tarptautinius kokybės standartus. Didelis kokybės šuolis įvyko gaminant titaninius varžtus ir kaiščius, kurie sudaro protezus. Pagaminti iš titano lydinių, šie protezai naudojami dantų vainikams, ortodontiniams prietaisams ir protezams pritvirtinti žandikaulio ir žandikaulio kauluose “. (Jornal do Brasil, 1996 m. Spalio mėn.)
Atsižvelgiant į tai, kad titano atominis skaičius yra 22, jo elektroninė konfigūracija bus:
a) 1s2 2s2 2p6 3s2 3p3
b) 1s2 2s2 2p6 3s2 3p5
c) 1s2 2s2 2p6 3s2 3p6 4s2
d) 1s2 2s2 2p6 3s2 3p6 4s2 3d2
e) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6
Teisinga alternatyva: d) 1s2 2s2 2p6 3s2 3p6 4s2 3d2.
Linuso Paulingo elektronų pasiskirstymo titane diagrama yra:
2 klausimas
(ACAFE) Atsižvelgiant į bet kurį bendrą M elementą, kuris turi 1s elektroninę konfigūraciją2 2s2 2p6 3s2 3p6 4s2 3d5, galima sakyti, kad:
Aš jo atominis skaičius yra 25;
II. paskutiniame apvalkale yra 7 elektronai;
III. turi 5 neporinius elektronus;
IV. priklauso 7A šeimai.
Teiginiai yra teisingi:
a) tik I, II ir III
b) tik I ir III
c) tik II ir IV
d) tik I ir IV
e) tik II, III ir IV
Teisinga alternatyva: b) tik I ir III.
Aš TEISINGA Suskaičiavę elektronų skaičių elektroniniame skirstinyje matome, kad buvo naudojami 25. Taigi, atominis skaičius yra 25 ir atitinka cheminį elementą manganas.
II. NETEISINGAI. Paskutinis sluoksnis, ty išorinis sluoksnis, turi 2 elektronus, tai yra 4-ieji2.
III. TEISINGA Nesuporuoti elektronai yra d pakopoje, kurioje telpa iki 10 elektronų, tačiau elektroniniame mangano skirstyme antriniam lygiui priskirti tik 5 elektronai.
IV. NETEISINGAI. Manganas yra 7B šeimoje ir 4-ame laikotarpyje.
3 klausimas
(UFSC) Elektronų skaičius kiekviename stroncio atomo pakopoje (38Sr) didėjančia energijos tvarka yra:
a) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2
b) 1s2 2s2 2p6 3s2 3p6 4s2 4p6 3d10 5s2
c) 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 5s2
d) 1s2 2s2 2p6 3s2 3p6 4p6 4s2 3d10 5s2
e) 1s2 2s2 2p6 3p6 3s2 4s2 4p6 3d10 5s2
Teisinga alternatyva: a) 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2.
Linuso Paulingo stroncio elektronų pasiskirstymo diagrama yra:
Patikrinkite savo žinias dar daugiau! Taip pat išspręskite:
- Elektroninio platinimo pratybos
- Periodinės lentelės pratimai