Elementai pavadinti šarminių žemių metalai yra tie, kurie priklauso periodinės lentelės 2 arba IIA šeimai. Tokią grupę sudaro šie cheminiai elementai: Būkite (berilis), Mg (magnis), Ca (kalcis), Sr (stroncis), Ba (baris) ir radis (Ra).

Jie turi du elektronus valentiniame apvalkale, o jų bendrą pasiskirstymą žymi ns2, kur ne žymi paskutinio lygio skaičių. Dėl šios savybės jie yra linkę prarasti šiuos du elektronus, todėl atsiranda 2+ krūvio katijonai.
Terminas „žemė“ reiškia „egzistuojančią žemėje“, nes būtent čia šie elementai yra daugiausia mineraluose. Pavyzdžiui, kalcis kalcio fosfato junginio (Ca3(Dulkės4)2), yra žemės plutoje ir tarnauja kaip žaliava gaminant fosforą. Jo taip pat yra gyvūnų kauluose, todėl, kai šie kalcinuojami, gaunamas vadinamasis „kaulų miltai“, kuriuose yra kalcio fosfato.
Tarp šarminių žemės metalų labiausiai išsiskiria Kalcis tai Magnis.
- Kalcis
Kalcio jonas (Ca2+) yra apie 90% mūsų kaulų ir dantų; o gyvūnuose jo yra ir jų lukštuose. Jo funkcija yra stiprinti kaulų struktūrą ir tarnauti kaip raumenų relaksantas. Trūkstant kalcio organizme, gali atsirasti raumenų mėšlungis, stabligė ir osteoporozė. Štai kodėl svarbu jį valgyti per maistą, kuriame gausu kalcio, pvz., Pieną ir jo darinius (sviestą, sūrį ir kt.), Mėsą ir daržoves.
Kita vertus, per didelis kalcio kiekis gali sukelti raumenų atsipalaidavimą, inkstų akmenis ir kaulų skausmus.
Be minėtų maisto produktų, kalcio vis dar yra daugelyje gamtos vietų, ypač mineraluose, tokiuose kaip kalcitas (CaCO3) arba kalcio karbonatas, kuris yra kalkakmenio ir marmuro sudedamoji dalis, o marmuras naudojamas kriauklėms, statuloms, grindims ir laiptinėms gaminti. Kalcio karbonatas taip pat yra stalaktitų ir stalagmitų urvuose statybininkas. Kalcio yra ir natūraliame gipse (CaSO4. 2 valandos2O), vadinamas gipsu. Ši druska gali būti dehidratuojama ir sukelti CaSO4 bevandenis, tai yra mokyklinė kreida.
Pramonėje gaminamos pirmojo kalkės (CaO), gesintos kalkės, dar vadinamos hidratuotomis arba gesintomis kalkėmis, kurios iš tikrųjų yra kalcio hidroksidas (Ca (OH)2), naudojamas balinant dažus ir ruošiant skiedinį. Švelnus gipso kaitinimas leidžia gauti statybose naudojamą hemihidratuotą kalcio sulfatą, kuris yra gipsas. pilietinė visuomenė, gamindama pelėsius odontologijoje ir medicinoje, kad apsaugotų kaulų lūžius, pvz., žemiau parodyta rankoje.
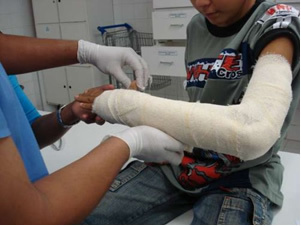
- Magnis
jonas magnis jis taip pat turi didelę biologinę reikšmę, nes jo yra 70% mūsų kaulų, o tai skatina fermentų, raumenų ir judėjimo koordinaciją. Jo trūkumas organizme gali sukelti dezorientaciją, hipertenziją, drebulį ir silpną pulsą. Todėl turėtume valgyti šiuos maisto produktus, kuriuose yra šio elemento: riešutus, grūdus ir žalias daržoves. Be to, magnio perteklius organizme gali sukelti mieguistumą.
Magnis taip pat yra jūros vandenyje ir mineraluose. Jis naudojamas metaliniuose lydiniuose, tokiuose kaip aukos metalai (kurie oksiduojasi vietoj plieno, užkertant kelią jo korozijai), „magnio“ ratukuose ir fejerverkuose (siūlantys sidabro ir baltos spalvos). Labai svarbus magnio junginys yra magnio hidroksidas (Mg (OH)2), kuris, paskleidus vandenyje, esant maždaug 7% koncentracijai, sudaro žinomą suspensiją populiariai kaip magnezijos pienas, kuris veikia kaip antacidas, kovojantis su skrandžio rūgštingumu (rėmuo) ir kaip vidurius laisvinantis.

Jennifer Fogaça
Baigė chemiją
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/metais-alcalinoterrosos.htm


