Izomerija tai yra natūralus reiškinys, kai skirtingų medžiagų (atsižvelgiant į chemines ir fizines savybes) molekulinė formulė yra tokia pati kaip šiame pavyzdyje:
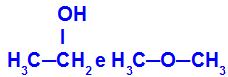
Skirtingos medžiagos, turinčios tą pačią molekulinę formulę
Etanolis (kairėje) turi molekulinę formulę C2H6O, kuris taip pat pasitaiko su metoksietanu (dešinėje), taigi jie yra izomerai.
Izomerijos tipai
→ plokščias izomeras
Būtent izomerijos tipas tiria struktūrinius izomerų skirtumus.
) Okupacija
Tai plokščiosios izomerijos tipas, kai medžiagų skirtumas yra pagrįstas skirtumu tarp organinių funkcijų, kurioms jos priklauso. Žr. Keletą pavyzdžių:
Propanonas ir propanas:
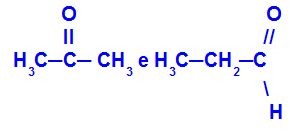
Izomerai, priklausantys skirtingoms funkcijoms
Propanonas (kairėje) priklauso ketonų grupei, o propanalas (dešinėje) priklauso aldehido grupei.
B) Kalėjimas
Tai plokščiosios izomerijos tipas, kai medžiagų skirtumas yra pagrįstas skirtumu tarp jų esančių grandinių. Žr. Pavyzdį:
2-metil-propanas ir butanas
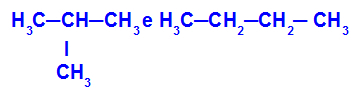
Izomerai, turintys skirtingos klasifikacijos grandines
Pavyzdyje galime pamatyti, kad 2-metil-propanas (kairėje) turi šakotą grandinę, o butanas (dešinėje) - normalią grandinę.
ç) Pozicija
Tai plokščiosios izomerijos tipas, kai medžiagų skirtumas yra pagrįstas komponentų, esančių jų grandinėse, padėties skirtumu. Žr. Pavyzdį:
1-chlor-propanas ir 2-chlor-propanas
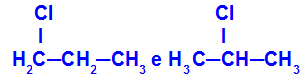
Izomerai, kurių komponentai yra skirtingose grandinės vietose
Pavyzdyje galime pamatyti, kad 1-chlor-propane (kairėje) chloras yra ant anglies 1, o 2-chlor-propane (dešinėje) chloras yra ant anglies 2.
d) Metameria arba kompensacija
PASTABA: Izomerija galioja tik heterogeninėms stygoms.
Tai plokščiosios izomerijos tipas, kai medžiagų skirtumas yra pagrįstas heteroatomo, esančio jų grandinėse, padėties skirtumu. Žr. Pavyzdį:
Pavyzdys: Metoksipropanas ir etoksietanas
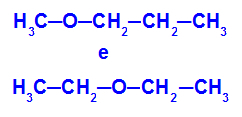
Izomerai, turintys heteroatomus skirtingose grandinės vietose
Pavyzdyje galime pamatyti, kad metoksipropane (kairėje) deguonis turi radikalą, kurio vienoje pusėje yra viena anglis, kitoje - trys angliai. Etoksietane (dešinėje) deguonis turi radikalą, kurio vienoje pusėje yra du angliai, kitoje - du angliai.
ir)Tautomery
Tai yra konkretus plokštumos funkcijos izomerijos atvejis, kuris pasireiškia tik trimis organinėmis funkcijomis:
Aldehidas
ketonas
Enol
Šio tipo izomerija veikia dėl to, kad tarp enolio ir aldehido bei tarp enolio ir ketono yra cheminė pusiausvyra, tai yra, šie komponentai nuolat virsta vienas kitu. Žr. Pavyzdį:
Prop-2-en-1-olis ir propanonas
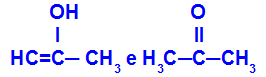
Izomerai, priklausantys skirtingoms funkcijoms
Pavyzdyje galime pamatyti, kad Prop-2-en-1-olis (kairėje) priklauso enolių grupei, o propanonas (dešinėje) priklauso ketonų grupei, taigi jie yra tautomerijos izomerai.
→ Kosmoso izomerija
Tai izomerijos tipas, apibrėžtas molekulinės erdvinės analizės.
a) geometriniai izomerai
Nesustokite dabar... Po reklamos yra daugiau;)
Tai yra erdvinės izomerijos tipas, atsirandantis, kai medžiaga turi molekulių, turinčių šias charakteristikas:
Uždara grandinė, turinti du angliavandenilius su dviem skirtingais ligandais, kaip parodyta toliau pateiktame pavyzdyje:

Uždara struktūra su geometrine izomerija
Atvira grandinė, turinti dvigubą jungtį tarp anglies junginių ir kiekviename iš šių dvigubos jungties anglių yra du skirtingi ligandai, kaip parodyta toliau pateiktame pavyzdyje:
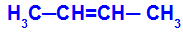
Atvira struktūra su geometrine izomerija
Geometrinė izomerija skirstoma į dvi grupes:
1O Grupė: cis-trans
Jis įvyksta, kai du vienos anglies ligandai yra griežtai lygūs dviem kitos anglies ligandams, nesvarbu, ar jie yra atviroje, ar uždaroje struktūroje.
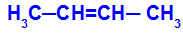
Medžiagos, turinčios cis-trans izomeriją, grandinė
Izomeras bus vadinamas cis, kai tie patys ligandai yra toje pačioje plokštumoje.

Cis izomero pavyzdys
Izomeras bus vadinamas trans, kai skirtingi ligandai yra toje pačioje plokštumoje.

Trans izomero pavyzdys
2O Grupė: E-Z
Jis atsiranda, kai du vienos anglies ligandai yra skirtingi, palyginti su dviem kitos anglies ligandais, arba atviroje, arba uždaroje struktūroje.

Medžiagos, turinčios E-Z izomerizmą, grandinė
Izomeras bus vadinamas E, kai didžiausią atomų skaičių turintys ligandai yra priešingose plokštumose. Toliau pateiktame pavyzdyje kairėje esanti anglis turi didžiausią atominį skaičių Br (35), o kitame yra deguonis (8).
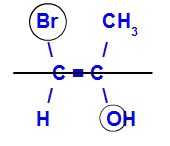
E-izomero pavyzdys
Izomeras bus vadinamas Z, kai didžiausią atomų skaičių turintys ligandai yra toje pačioje plokštumoje. Toliau pateiktame pavyzdyje kairėje esanti anglis turi didžiausią atominį skaičių Br (35), o kitame yra deguonis (8).

Z-izomero pavyzdys
B) optinis izomeras
Tai yra erdvinės izomerijos tipas, atsirandantis tik tuo atveju, jei medžiaga turi molekulių su chiralinė anglis (tas, kuriame yra keturi skirtingi ligandai) jų struktūrose. Molekulė su chiraline anglimi turi galimybę poliarizuoti ir nukreipti šviesą taip:
Dešinėje (dešinysis izomeras)
Kairėje (pasukamas izomeras)
Optinio aktyvumo junginys visada turi aktyvūs izomerai (vadinami optiniais antipodais) ir neaktyvūs izomerai (dviejų aktyvių izomerų mišinys, mišinys vadinamas raceminiu).
Chiralinės anglies turinčio junginio aktyviųjų (IOA) ir neaktyviųjų (IOI) izomerų skaičiui nustatyti galime naudoti šią formulę:
IOA = 2ne
IOI = 2ne
2
Žemiau pateikiamas junginio, turinčio geometrinį izomerizmą, pavyzdys:
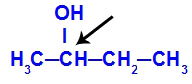
Chiralinė anglis yra butan-2-olyje
Butan-2-olio struktūra turi šiuos ligandus:
Metilas (CH3)
Etilas (CH3-CH2)
Vandenilis (H)
Hidroksilas (OH)
Todėl butan-2-olis turi tik vieną chiralinę anglį:
Aktyvūs izomerai:
IOA = 21
IOA = 2
Neaktyvūs izomerai:
IOI = 21
2
IOI = 2
2
IOI = 1
Mano. Diogo Lopes Dias
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
DIENOS, Diogo Lopes. "Kas yra izomerija?"; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-isomeria.htm. Žiūrėta 2021 m. Birželio 27 d.