Tirpalas yra homogeniškas dviejų ar daugiau medžiagų mišinys.. Kaip, pavyzdžiui, druskos (ištirpusios medžiagos) tirpalas, ištirpintas vandenyje (tirpiklyje).

Šis procesas ypač svarbus chemijos laboratorijose ir pramonėje, nes chemikas turi paruošti žinomos koncentracijos tirpalus. Be to, eksperimentinėje veikloje naudojami labai mažos koncentracijos tirpalai, todėl koncentruoto tirpalo mėginys praskiedžiamas iki norimos koncentracijos.
Kasdien, kelis kartus, patys to nesuprasdami, atliekame tirpalų skiedimo procesą. Pavyzdžiui, valymo ir buities higienos priemonių, tokių kaip dezinfekcijos priemonės, pakuotėse patariama jas prieš naudojimą atskiesti. Kai kurie gamintojai siūlo produktų etiketėse praskiesti vandeniu santykiu nuo 1 iki 3, tai yra, kiekvienai produkto daliai reikia pridėti 3 dalis vandens. Tai daroma todėl, kad produktas yra labai koncentruotas ir stiprus ir gali būti pažeistas jo naudojimo vietoje, jei jis nebus praskiestas tinkamu būdu. Kita vertus, atskiedus daugiau, nei turėtų, galite prarasti pinigų, nes produktas nepasieks norimo rezultato.

Kitas pavyzdys - kai gaminame sultis. Daugelio sulčių koncentratų etiketėse nurodoma, kad stiklinę sulčių reikia praskiesti arba sumaišyti su 5 stiklinėmis vandens. Taigi sultys tampa „silpnesnės“, tai yra, mažiau koncentruotos.
Nesustokite dabar... Po reklamos yra daugiau;)
Įsivaizduokite, kad tokias sultis atskiedėte 3 L vandens. Jei pradinė sulčių koncentracija buvo 40 g / l, tai reiškia, kad kiekvienam tirpiklio litrui buvo 40 g masės. Bet kadangi turėsime 3 l, masė bus padalinta iš 3 ir kiekvieno litro tirpalo koncentracija bus maždaug 13, 33 g / l arba 13 gramų. Tačiau visame tirpale vis tiek išlieka 40 g ištirpusios medžiagos masė.
Šią naują koncentraciją galima apskaičiuoti taip:
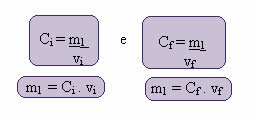
Kur indeksai i ir f reiškia atitinkamai pradinę ir galutinę reikšmes. Kadangi m1 reikšmė nepasikeitė, galime išlyginti lygtis:
Çi. vi = Cf. vf
Pagal ankstesnį pavyzdį pakeisdami turimas vertes, atkreipkite dėmesį:
Pradinis sprendimas:
Çi: 40 g / l
m1: 40g
vi: 1L
Galutinis sprendimas:
Çf: ?
m1: 40g
vf: 3L
Çi. vi = Cf. vf
(40 g / l). (1 L) = Cf. 3L
Çf = 40 g / l
3
Çf = 13,333 g / l
Tas pats argumentas galioja ir molinei koncentracijai (M) bei ištirpusios medžiagos arba titro masės procentui (T):
Mi. vi = Mf. vf ir Ti. vi = T.f. vf
Jennifer Fogaça
Baigė chemiją
Brazilijos mokyklos komanda
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
FOGAÇA, Jennifer Rocha Vargas. „Tirpalų skiedimas“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/diluicao-solucoes.htm. Žiūrėta 2021 m. Birželio 27 d.