
Kartais taip gali atsitikti minimali formulė būti toks pat kaip junginio molekulinė formulė; tačiau tai ne visada tiesa.
Pavyzdžiui, empirinė arba minimali vandens formulė yra H2O, nurodant, kad tarp vandens molekules sudarančių elementų yra 2: 1 santykis. Taip sutapo ir molekulinė vandens formulė. Tačiau norėdami pamatyti, kad taip nutinka ne visada, pažiūrėkite į du toliau pateiktus pavyzdžius:
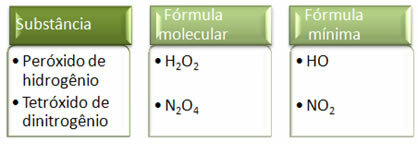
Kadangi minimali formulė yra tik kiekvieno elemento atomų santykis, o ne faktinis jų kiekis molekulinėje formulėje, tai gali atsirasti skirtingų junginių, turinčių tą pačią empirinę formulę ir net minimalią junginio formulę, gali būti tokie patys kaip molekulinės formulės kita. Atkreipkite dėmesį, kaip tai gali įvykti toliau pateiktame pavyzdyje:
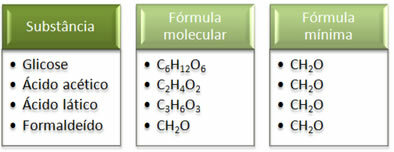
Pažiūrėkite, ar minimali formulė CH2Visoms medžiagoms tas pats, tai yra, ši minimali formulė išreiškia, kad visais atvejais anglies, vandenilio ir deguonies atomai yra molekulinėse formulėse santykiu 1:2:1. Be to, vienintelis, kurio molekulinė formulė yra tokia pati kaip empirinės formulės, yra formaldehidas.
- Minimalios arba empirinės formulės apskaičiavimas:
Norint nustatyti junginio empirinę formulę, pirmiausia reikia žinoti, kokia yra jo procentinė arba artima formulė. Tai galima padaryti matuojant kiekvieno elemento masę 100 g mėginio. Tekstas "Procentinė arba „Centesimal“ formulė“Paaiškina šį klausimą geriau.
Nesustokite dabar... Po reklamos yra daugiau;)
Pvz., Tarkime, kad artimą tam tikro junginio sudėtį sudaro: 40,00% C, 6,67% H ir 53,33% O. Mes perduodame šias vertes gramais, atsižvelgiant į 100 g junginio mėginio masę. Taigi turime: 40 g C, 6,67 g H ir 53,33 g O.
Dabar būtina šias vertes perduoti medžiagos kiekiui (mol). Mes tai darome padalijant kiekvieną iš rastų verčių iš jų atitinkamų molinių masių:
C: 40/12 = 3,33
H: 6,67 / 1 = 6,67
O: 53,33 / 16 = 3,33
Kadangi reikšmės nėra sveiki skaičiai, mes naudojame šį įrenginį: visas vertes padalijame iš mažiausios iš jų, kad proporcija tarp jų nepakistų.
Šiuo atveju mažiausia vertė yra 3,33, taigi rezultatas bus:
C: 3,33 / 3,33 = 1
H: 6,67 / 3,33 = 2
O: 3,33 / 3,33 = 1
Taigi minimali šios nežinomos medžiagos formulė yra lygi: Ç1H2O1 arba CH2O.
Trumpai tariant, reikia nustatyti empirinę ar minimalią medžiagos formulę:

Jennifer Fogaça
Baigė chemiją
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
FOGAÇA, Jennifer Rocha Vargas. „Minimali arba empirinė formulė“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/formula-minima-ou-empirica.htm. Žiūrėta 2021 m. Birželio 28 d.


