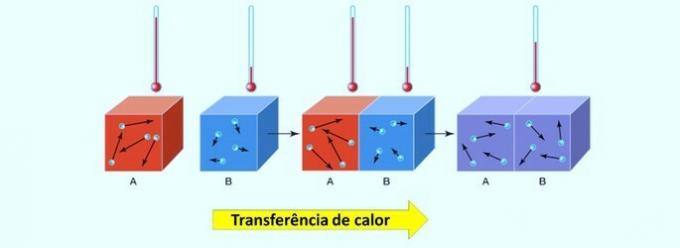
Radioaktyvumas yra savybė, kuri patinka kai kuriems atomams uranas ir radijas, turi išleisti spontaniškai energijos formos dalelės ir banga, tampa cheminiai elementai stabilesnis ir lengvesnis.
Tipai
Radioaktyvumas prisistato du keliai skirtingi spinduliavimai: dalelė - alfa (α) ir beta (β); ir elektromagnetinės bangos - gama spinduliai (γ).
alfa spinduliai: tai teigiamos dalelės, sudarytos iš dviejų protonų ir dviejų neutronų ir turinčios mažą skvarbos galią.
beta spinduliaiyra neigiamos dalelės, kuriose nėra elektrono turinčios masės (nereikšminga masė), o jų skvarbos galia yra didesnė nei alfa spindulių, bet mažesnė nei gama spindulių.
Gama: jie yra didelės energijos elektromagnetinės bangos ir, kadangi jie nėra dalelės, jie taip pat neturi masės.
Skaityk ir tu: Radioaktyvumo formulės
Nesustokite dabar... Po reklamos yra daugiau;)
įstatymai
Radioaktyvioji dalelių emisija atitinka tam tikrą elgesį, kuris paaiškinamas radioaktyvumas (vienas alfa daliai ir vienas beta dalelei), kuriuos aprašė chemikas Anglų Frederickas Soddyo lenkų chemikas ir fizikas Kazimierz Fajans.
Pirmasis radioaktyvumo dėsnis
Pagal šį dėsnį, kai radioaktyvus atomas skleidžia alfa tipo spinduliuotę, jis sukels a naujas atomas su šerdimi du protonai ir du neutronai mažiau, iš viso masė keturi vienetai mažesni. Pirmąjį radioaktyvumo dėsnį galime pavaizduoti tokia bendrine lygtimi:
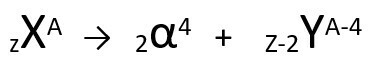
Pirmojo radioaktyvumo dėsnio bendroji lygtis.
Pažvelkime į pavyzdį:
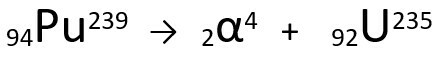
Plutonio-239 α dalelių emisijos lygtis.
Atkreipkite dėmesį, kad skleidžiant alfa spinduliuotę, naujai susiformavusio atomo Urano-235 masė yra keturi vienetai mažesni ir atomo numeris dviem mažesniais vienetais - tiksliai tokios vertės, kurios atitinka α dalelę, kurią skleidžia branduolys plutonis. Norėdami sužinoti daugiau apie tai, eikite į: Pirmasis radioaktyvumo įstatymas arba pirmasis Soddy įstatymas.
Antrasis radioaktyvumo dėsnis
Antrasis įstatymas kalba apie beta versija. Kai atomas skleidžia beta dalelę, susidedančią iš elektrono ir nereikšmingos masės, jos atominė masė lieka nepakitęs tai tavo atominis skaičius padidina vieną vienetą. Paprastai mes atstovaujame taip:
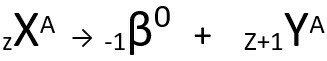
Antrojo radioaktyvumo dėsnio bendroji lygtis.
Žr. Pavyzdį:
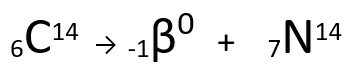
Lygtis, vaizduojanti anglies-14 β dalelių emisiją.
Galima pastebėti, kad susidariusio azoto atomo masė yra tokia pati kaip C-14 atomo, tai yra jie yra izobarai, o jo atominis skaičius padidėja vienu vienetu. Padidėjimas atominis skaičiuspaaiškino mokslininkas Henrico Fermi, kuris pasiūlė vieną iš neutronai branduolio yra transformuojamas pagal šią lygtį, generuojant aelektronas(skleidžiama beta dalelė), a neutrino(subatominė dalelė be elektrinio krūvio ir masės) ir a protonas(P).
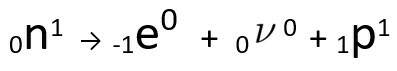
Lygtis, vaizduojanti neutronų transmutaciją, pagal Fermi hipotezę.
O elektronas tai neutrino yra išduodami iš pagrindo, likę tik protonas, kuris paaiškina atominio skaičiaus padidėjimą. Norėdami sužinoti daugiau apie tai, eikite į: Antrasis radioaktyvumo įstatymas arba antrasis Soddy įstatymas.
Taip pat skaitykite: Radioaktyviosios taršos ir švitinimo skirtumas
programos
nepaisant neigiamas požiūris tą radioaktyvumo indėlį jis turi svarbios programos pavyzdžiui, kasdieniame mūsų gyvenime gamyba elektrosį atominės elektrinės per dalijimasisradioaktyviųjų atomų.
Šiuo metu Brazilija nenaudoja atominė energija kaip pagrindinį energijos šaltinį, tačiau jis turi atomines elektrines (Angra 1 ir 2), kurios teikia energiją šaliai. Taip pat galime paminėti medžiagos pažintys archeologai rado naudodamiesi anglies-14.

Rio de Žaneiro atominė elektrinė, Brazilija
Kitas pagrindinis radioaktyvumo vaidmuo yra susijęs su medicinos sritimi, pavyzdžiui, atliekant tyrimus Rentgeno spinduliaiir KT tyrimai, taip pat kai kurių tipų vėžio gydymas.
Skaityk ir tu: Pagrindinė branduolinės energijos gamybos rizika aplinkai
natūralus radioaktyvumas
kasdien mes veikiami The maži kiekiai dirbtinės ar natūralios radiacijos. Natūralus radioaktyvumas gamtoje atsiranda savaime. Dalis šios radiacijos, kurią gauname, gaunama iš kasdien suvartojamo maisto, pavyzdžiui, Radonas-226 ir Kalis-40, kurie pateikiami labai žemas lygis jie nekelia pavojaus mūsų sveikatai ir nekenkia maisto produktų maistinėms vertėms.
Šis procesas yra skirtas radioaktyviųjų medžiagų išmetimui į aplinką išsaugoti maistą ir skatinti a augalų augimas. Keli radiaciją skleidžiančių maisto produktų pavyzdžiai: Braziliški riešutai, bananas, pupelės, raudona mėsa, be kita ko.
Atradimas
Radioaktyvumo tyrimas prasidėjo vokiečių fiziko atliktais tyrimais Vilhelmas Röentgenas, 1895 m., kai jis tyrė poveikisliuminescencija. Kitas svarbus radioaktyvumo vystymosi mokslininkas buvo prancūzų fizikas Antoine'as-Henri'as Becquerelis, kuris 1896 m. pastebėjo žymes, padarytas ant fotofilmų pagal urano druskos pavyzdį.
Tačiau tai buvo Kiuri pora kurie pirmą kartą vartojo radioaktyvumo terminą. Į 1898, lenkų Marie Curie tęsė radioaktyvumo tyrimus ir padarė vertingų atradimų šioje srityje, pavyzdžiui, atrado du naujus radioaktyviuosius elementus: polonį (Po) ir radį (Ra).
Užpakalyje, Ernestas Rutherfordas atrado alfa tipo spinduliuotę (α) ir beta (β), leidusį geriau paaiškinti jo atominį modelį, taip pat pažengti su radioaktyvumu susijusius tyrimus.
Taip pat skaitykite:Marie Curie: biografija, indėliai ir palikimas
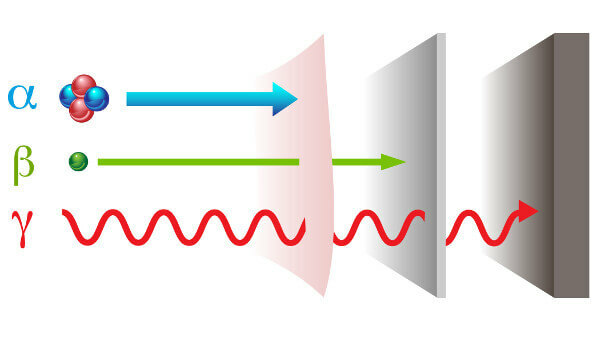
Spinduliuotės rūšys ir jų skverbimosi galios.
irimas
O radioaktyvusis skilimas (arba transmutacija) yra natūralus procesas kur vienas nestabili šerdis skleidžia radiaciją, iš eilės, siekiant sumažink savo energiją ir tampa stabilūs.
Paprastai tai įvyksta su atomo skaičiaus atomais. didesnis nei 84, kurie yra atomai su didelis nestabilumas branduolį dėl branduolyje susikaupusio teigiamo krūvio (protonų) kiekio. Šiame procese neutronų nepakanka stabilizuoti visus branduolyje susitelkusius protonus, o tada branduolys pradeda radioaktyviai irti, kol jo atominis skaičius bus mažesnis nei 84.
Kai kuriais atvejais gali atsitikti taip, kad atomai, kurių atomų skaičius yra mažesnis nei 84, turi nestabilius branduolius pereiti skilimo procesą, tačiau tam jie turi turėti daug protonų, gerokai viršijančių protonų skaičių neutronai.
Radioaktyvus skilimas yra apskaičiuojamas pagal pusinės eliminacijos periodą (arba pusiau suirimo laikotarpis, P) radioizotopas, kuris yra laikas, per kurį pusė pradinio radioaktyvaus mėginio masės suyra, ty tampa stabili. Grafiškai kalbant, pusinės eliminacijos laikas yra pateiktas žemiau. Nes tai yra a tęstinis procesas, kreivė linkusi siekti nulis.
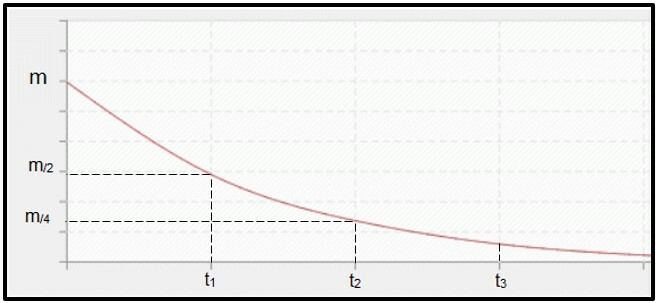
Grafikas, rodantis pusinės eliminacijos laiką.
Apskaičiuojant radioaktyvųjį skilimą, naudojamos šios formulės:
Po pusinės eliminacijos periodo likusios masės apskaičiavimo formulė:
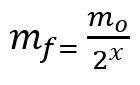
mf - galutinė masė
mO - pradinė masė
x - praėjo pusinės eliminacijos laikas
Radioaktyviojo mėginio suirimo laiko apskaičiavimo formulė:
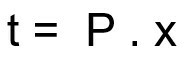
t - irimo laikas
P - pusinės eliminacijos periodas
x - praėjo pusinės eliminacijos laikas
radioaktyviųjų elementų
Yra dviejų tipų radioaktyviųjų elementų: tu natūralus ir dirbtinis. Natūralūs turi gamtoje randamų elementų, jau turinčių nestabilų šerdį, pavyzdžiui, uranas, O aktiniumas tai radijas. Dirbtiniai gaminami procesais, kurie destabilizuoja atomo branduolį. Šiuo atveju galime paminėti astatinas tai francium.
Pagrindiniai radioaktyvieji elementai yra šie: uranas-235, kobaltas-60, stroncis-90, radis-224 ir jodas-131. Dėl plataus naudojimo atominėse elektrinėse ir vėžio gydymui šie elementai dažniausiai pasirodo mūsų kasdieniame gyvenime. Norėdami sužinoti daugiau apie šią temą, eikite į: radioaktyviųjų elementų.
Radioaktyvios šiukšlės
Radioaktyviosios atliekos arba radioaktyvios atliekos tai likučių iš pramonės šakose kurie savo procesuose naudoja radioaktyviąsias medžiagas, kurios nebeturi praktinio taikymo. Ši šiukšlė daugiausia kyla iš atominės elektrinės tai iš medicinoje.
Didelė radioaktyviųjų atliekų gamyba buvo a aplinkos problema visam pasauliui dėl nedaug ir nepakankamai šalinimo sąlygos ir saugojimas.
Šios atliekos yra susijusios su dirvožemio, vandens kelių ir oro užteršimu, dėl kurio aplinkos naikinimas palaipsniui. Be to, jie taip pat kelia pavojų žmonių sveikatai, pvz infekcijos, vėžys ir sunkesniais užteršimo atvejais jie gali sukelti mirtis.
sprendė pratimus
(PUC-Camp-SP) Atominės bombos, dar vadinamos branduoline bomba, dalijamoji sudedamoji dalis yra urano-235 atomai, , alfa dalelių skleidėjai
, alfa dalelių skleidėjai 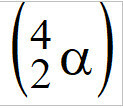 . Kiekvienas U-235 atomas, skleisdamas alfa dalelę, virsta kitu elementu, kurio atomo skaičius yra lygus
. Kiekvienas U-235 atomas, skleisdamas alfa dalelę, virsta kitu elementu, kurio atomo skaičius yra lygus
a) 231.
b) 233.
c) 234.
d) 88.
e) 90.
Šablonas: Kai atomas skleidžia alfa dalelę, pagal pirmąjį radioaktyvumo dėsnį atomo skaičius sumažėja dviem vienetais. Todėl: 92-2 = 90. Laiškas e.
(PUC-Camp-SP) Radioaktyvioji jodo įvairovė, vartojama medicinoje, jodo-125 pusinės eliminacijos laikas yra 60 dienų. Kiek gramų jodo-125 liks po šešių mėnesių, remiantis mėginiu, kuriame yra 2,00 g radioizotopo?
a) 1,50
b) 0,75
c) 0,66
d) 0,25
e) 0,10
Šablonas: Pirmiausia apskaičiuojamas pusinės eliminacijos laikas, praleistas per 180 dienų:
t = P. x
180 = 60. x
x = 3
Nustačius praėjusio pusinės eliminacijos periodų skaičių, apskaičiuojama masė, kuri liks po 180 dienų:
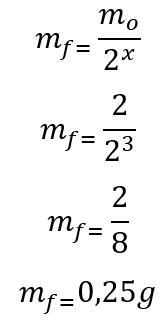
Todėl šešių mėnesių pabaigoje liks 0,25 g jodo-135 radioizotopo. D raidė
Autorius Viktoras Feliksas
Baigė chemiją