Elektrolizė tai nėra spontaniškas, tai yra, natūraliai nevykstantis procesas, kurio metu medžiagos susidaro elektrinio išlydžio būdu vandenyje ištirptuose ar ištirpintuose junginiuose. Šiame procese elektros srovė pasiekia stiklinį indą (elektrolitinį rezervuarą), kuriame yra du inertiniai elektrodai (kurie nenukenčia ar oksidacija nei sumažinimas) suformuota grafito ar platinos. Šie elektrodai yra prijungti prie elektros šaltinio (paprastai a būgnai) ir panardinti į druską ar bazę, išlydytą arba ištirpintą vandenyje. Visai kaip baterija, elektrolizė turi katodą (kur vyksta redukcija) ir anodą (kur vyksta oksidacija).
Santrauka
Elektrolizė yra nesavaiminis procesas;
Gali susidaryti paprastos arba sudėtinės medžiagos;
Tai gali pasireikšti ištirpusia ištirpusia medžiaga (magminė elektrolizė);
Tai gali pasireikšti ištirpusiu tirpalu vandenyje (vandeninė elektrolizė);
Katijonas katode visuomet redukuojamas;
Anijonas visada oksiduojasi anode.
Taip pat žiūrėkite:Aliuminio gavimas iš elektrolizės

Elektrolizės tipai
Tai yra elektrolizė, kuri įvyksta, kai ištirpusiam joniniam junginiui atliekama elektros iškrova. Joninis junginys susidaro iš joninio ryšio, pavyzdžiui, a druska arba a bazė neorganinis. Savo ruožtu kalbėdami apie išlydytą junginį turime omenyje junginį, kuris eina iš kietos į skystą būseną.
- magminės elektrolizės pavyzdys
Kai atliekame kalio chlorido (KCl) sintezę, ši druska vykdo disociacijos procesą, išskirdama kalio katijoną (K+) ir jodido anijoną (l-).

Kalio chlorido disociacijos lygtis
Elektros srovei su šiais jonais pasiekus elektrolitinę ląstelę, kalio katijonas redukuojamas, susidaro metalinis kalis (K), o jodido anijonas oksiduojasi, susidaro kietas jodas (I2).
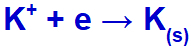
Kietojo kalio susidarymo lygtis
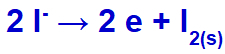
Kietojo jodo susidarymo lygtis
Tai yra elektrolizė, kuri įvyksta, kai elektrinė iškrova atliekama vandeniniame tirpale (turi vandens), kurį sudaro druska arba neorganinė bazė.
- Vandeninės elektrolizės pavyzdys
Kai vandenyje ištirpiname natrio chloridą, jis disocijuoja ir vanduo patiria jonizaciją:

Vandens jonizacijos ir natrio chlorido disociacijos lygtys
Kaip natrio katijonas (Na+) priklauso IA šeimai, hidronio katijonui (H+) praeina per išmetimą ir redukuojasi, susidaro vandenilio dujos (H2).
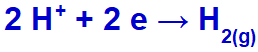
Vandenilio dujų susidarymo lygtis
Kaip chloridas (Cl-) nėra deguonies (neturi deguonies) ir nėra fluoras (F-), jis išleidžiamas, oksiduojasi ir susidaro chloro dujos (Cl2).

Chloro dujų susidarymo lygtis
Selektyvi jonų iškrova
Vykdant elektrolizės procesą vandeninėje terpėje (tirpale susidaro vanduo ir ištirpusios medžiagos), mes visada turėsime du katijonus: hidronį, iš vandens, ir bet kurį kitą, iš druskos disociacija (ištirpusios medžiagos pavyzdys). Mes taip pat turėsime du anijonus: hidroksilą, kuris gaunamas iš vandens, ir kitą - iš druskos.

Vandens jonizacijos ir druskos disociacijos jonai
- Selektyvus katijonų ir anijonų išleidimas
Jei ištirpusios medžiagos katijonas priklauso IA, IIA arba IIIA šeimai, hidronis (H+) bus sumažinta;
Jei kateteris, gaunamas iš tirpinio, nepriklauso aukščiau paminėtoms šeimoms, sumažės.
Jei ištirpusios medžiagos anijonas turi deguonies arba yra fluoras (F-), hidroksidas (OH-) bus oksiduojamasi;
-
Jei ištirpusios medžiagos anijonas neturi aukščiau nurodytų charakteristikų, jis oksiduojasi.
Nesustokite dabar... Po reklamos yra daugiau;)
Yra žinoma, kad vanduo gali savaime jonizuotis, gamindamas hidronio jonus (H+) ir hidroksidas (OH-), tačiau ši jonizacija yra gana ribota. Šį faktą įrodo gryno vandens neefektyvumas, vedant elektros srovę.
Toks kaip elektrolizė apima elektrinį išlydį, norint atlikti vandens elektrolizę, būtina ištirpinti ištirpusią medžiagą kuris palaiko selektyvų hidronio ir hidroksido išsiskyrimą (kaip matyti išleidimo temoje selektyvus).
Jei įpilame natrio sulfato (Na2TIK4), pavyzdžiui, viduryje turėsime natrio katijonus (Na+) ir hidronio (H+), taip pat hidroksido anijonus (OH-) ir sulfatas (SO4-2). Taigi, kai elektros srovė patenka į elektrolitinį baką:
hidronis bus išleistas, redukuojantis, nes natris priklauso IA šeimai;
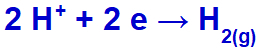
Vandenilio dujų susidarymo lygtis
hidroksidas bus išleistas, oksiduojamas, nes sulfato sudėtyje yra deguonies.
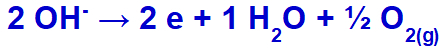
Deguonies dujų susidarymo lygtis
Kai iš vandens patekę du jonai (katijonas ir anijonas) buvo išleidžiami, sakome, kad įvyko vandens elektrolizė.
Taip pat žiūrėk: Kiekybiniai elektrolizės aspektai
Paprastų medžiagų, tokių kaip vandenilio dujos (H2), deguonies dujos (O2) ir tt;
Kompozicinių medžiagų, tokių kaip natrio hidroksidas (NaOH), sieros rūgštis (H2TIK4) ir tt;
Dalies padengimas tam tikru metalu, pavyzdžiui, variu (variu) ir auksu (padengimu auksu);
Naudokite tam, kad iš rūdos pašalintumėte tam tikrą metalą.
Išspręsti elektrolizės pratimai
1 pavyzdys - (Vunesp) Vandeninis CuCℓ tirpalas2 yra atliekamas elektrolizės naudojant platinos elektrodus. Teisingas teiginys yra:
a) Cu jonų redukcija įvyksta katode2+.
b) Cu jonų oksidacija vyksta anode2+.
c) Katode susidaro chloro dujos.
d) Platinos anodo dalis ištirpsta, susidaro Pt2+.
e) Šios elektrolizės produktai būtų kitokie, jei CuCl elektrolizė2 buvo ugninga (sintezė).
a) Teisingai. Kai CuCl2 yra ištirpęs vandenyje, turime hidronio katijonus (H+) ir vario II (Cu+2). Kadangi vario II katijonas nepriklauso IA, IIA ir IIIA šeimoms, jis yra sumažėjęs.
b) klaidinga, nes chloro anijonas (Cl) oksiduojamas anode-), kurio sudėtyje nėra deguonies ir kuris nėra fluoras (F-).
c) klaidinga, nes prie katodo vyksta vario II katijono redukcija, todėl susidaro vario metalas.
d) Klaidinga, kadangi platinos ar grafito elektrodai elektrolizės metu praleidžia tik elektrą, jie nedalyvauja procese.
e) klaidinga, kaip varinė chlorido II magminė elektrolizė (CuCl2) pateiktų tuos pačius produktus kaip ir vandeniniai, nes jonai būtų varis II (Cu+2) ir chloridas (Cl-1).
2 pavyzdys (UFRN) Apsvarstykite šias sistemas:
Aš Išlydytas natrio chloridas;
II. Natrio chlorido vandeninis tirpalas;
III. Lydyto natrio hidroksido;
IV. Natrio hidroksido vandeninis tirpalas.
Tie, kurie gali gauti natrio, kai jie yra elektrolizuojami, yra:
a) tik I ir II.
b) tik I ir III.
c) tik II ir IV.
d) tik III ir IV.
e) I, II, III ir IV.
Sistemos, kurios katode tiekia metalinį natrį, yra I ir III.
Aš - vienintelis terpėje esantis katijonas yra natrio katijonas, todėl tik jis gali redukuoti, susidarant metaliniam natriui.
II- Ši sistema nepateikia metalinis natris, nes natrio chloridas buvo ištirpęs vandenyje, todėl viduryje yra natrio katijonų (Na+) ir hidronio (H+) - tai yra tas, kuris patiria redukciją, nes natris priklauso IA šeimai.
III- Vienintelis terpėje esantis katijonas yra natrio katijonas (nes medžiaga buvo sulydyta), todėl tik jis redukuojamas ir susidaro metalinis natris;
IV- Ši sistema neteikia metalo natrio, nes natrio hidroksidas buvo ištirpintas vandenyje, todėl viduryje yra natrio katijonų (Na+) ir hidronio (H+) - tai yra tas, kuris patiria redukciją, nes natris priklauso IA šeimai.
Mano. Diogo Lopes Dias



