O amonio salietra yra kieta medžiaga molekulinės formulės NH4PRIE3 ir balta išvaizda (kai gryna). sudarė prie jonai NH4+ (amonio) ir NO3- (nitratas), nėra degi, tačiau yra labai oksiduojanti ir reaktinga. Jo skilimo reakcija gaminant susidaro didelis dujų kiekis, todėl netinkamas šio produkto laikymas tampa rimta problema, nes gali įvykti sprogimai. Ir taip pat plačiai naudojamas žemės ūkyje kaip trąša.
Taip pat skaitykite: Natūralios medžiagos - molekulės atsirado iš gamtos
Kas yra amonio nitratas?

Amonio nitratas tai druska kurį sudaro NH jonai4+ (amonio) ir NO3- (nitratas). Tai tvirtas junginys, kai grynas, jis yra baltos spalvos. Jis plačiai naudojamas kaip žemės ūkio trąša, tačiau taip pat gali būti naudojamas sprogmenų gamybai, kaip tai labai oksiduojanti medžiaga, tada oksiduojasi. Išbėgusi amonio nitrato reakcija sukelia didelį dujos, sukeliantis sprogstamasis poveikis.
Amonio nitrato charakteristikos
Molinė masė: 80,04336 g / mol.
Druska, sudaryta iš jonų: amonio (NH4+) ir nitratų (NO3-).
Išvaizda: balta kieta medžiaga.
Jis stipriai oksiduojasi.
Lengvai reaguoja su kitomis medžiagomis.
Jis nėra degus.
Normalioms temperatūros ir slėgio sąlygoms:
- tankis: 1,73 g / cm³;
- virimo temperatūra: 210 ° C;
- lydymosi temperatūra: 169,6 ° C;
- tirpumo vandenyje laipsnis: 216 g / 100ml;
- pH: 5,5 (0,2 M).
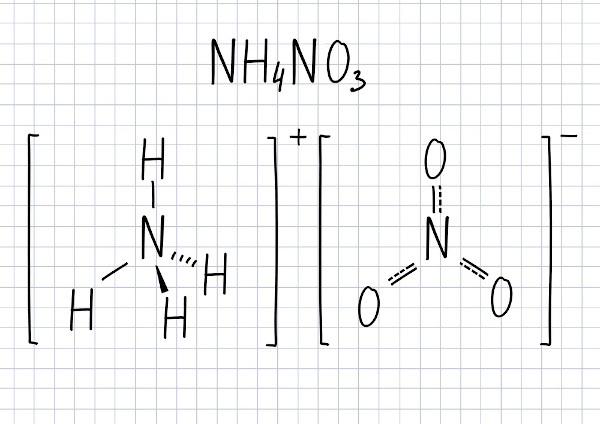
Amonio nitrato formulė
Šio junginio molekulinė formulė yra NH4PRIE3.
Amonio nitrato skaidymas
už tai, kad esi a medžiaga, pasižyminti dideliu reaktyvumu ir dideliu oksidavimo potencialu, amonio salietra, veikiama aukštoje temperatūroje, sukelia a irimo reakcija, o pagrindiniai produktai yra dujos, azotas, deguonies ir vandens garai. Skilimas atliekamas dviem etapais:
→ 1 žingsnis:
2NH4PRIE3 (s) → 2N2O (g) + 4H2O (g)
→ 2 etapas:
2N2O → 2N2g) + O2g)
→ Visuotinė lygtis:
2NH4PRIE3 (s) → 2N2g) + O2(g) + 4H2O (g)
Atkreipkite dėmesį, kad pirmojoje lygtyjevienas iš produktų gaunamas skaidant yra azoto oksidas (N2O), taip pat žinomas kaip juoko dujos. Jis naudojamas siekiant padidinti automobilių variklių galią deginti degalus ir kaip anestetiką, daugiausia - odontologų. Tai taip pat viena iš pagrindinių dujų, atsakingų už šiltnamio efektas.
Taip pat žiūrėkite: Kokios yra cheminių reakcijų rūšys?
Amonio nitrato gamyba
Amonio nitratą galima gauti reakcija tarp amonio sulfato (NH4)2TIK4 ir kalcio nitratas Ca (NO3)2. Žiūrėkite žemiau:
(NH4)2TIK4 + Ca (NE3)2 → 2 NH4PRIE3+ Byla4
Jis taip pat gali būti gaminamas iš dujinio amoniako, kuris burbuliuoja azoto rūgšties tirpale, kurio reakcijos produktas yra vandeninis amonio nitratas. Pažvelk:
NH3 g) + HNO3 (aq) → NH4PRIE3(čia)
Amonio nitrato naudojimas

- Trąšų gamyba
- Sprogmenys kasyklose, karjeruose ir statybose
- Herbicidai ir insekticidai
- Azoto oksido gavimas pramoniniam naudojimui
- Absorbentai oksidams
- Oksidantas raketoms
- Izoterminių maišelių gamyba
- Anestezinių dūmų gamyba, naudojant bitininkystės avilius
Taip pat prieiga: Kaip gesinti ugnį?
Amonio nitrato pavojai
Viena iš pagrindinių su amonio nitratu susijusių rizikų yra netinkamas saugojimas. Kadangi tai yra labai oksiduojanti medžiaga ir ji reaguoja su keliais kitais junginiais, ji sukelia a reakcija išsiskiriant dideliam dujų kiekiui. Netinkamas laikymas priklauso nuo užteršimo degiais produktais, šilumos ar dujų sulaikymo, kas gali sukelti sprogimus.
Tai jau įvyko Teksase, JAV, pavyzdžiui, iš Prancūzijos atplaukusiu krovininiu laivu, gabenusiu 2086 t amonio nitrato. įvyko nelaimė 1947 m ir tapo žinoma kaip Teksaso miesto katastrofa. Dėl tragedijos žuvo 581 žmogus ir tai įvyko dėl gaisro, kurio nėra laive ir kuris pasiekė amonio krovinį, sukėlusį sprogimą.
Kitas pavyzdys buvo sprogimo seka kuris įvyko 2020 m. rugpjūčio 4 d Beiruto miestas, Libanas, mirus daugiau kaip 100 žmonių ir 5000 sužeistų. Sprogimo mastą lėmė grandinės reakcija, kai joje buvo laikoma 2750 tonų amonio nitrato.
Taip pat verta paminėti, kad amonio nitratas gali sukelti odos ir akių dirginimas ir, jei įkvepiama, kvėpavimo sutrikimai. Kraujotakoje medžiaga turi toksinę galią, nes reaguoja su kūno skysčiais, o šios reakcijos produktai, pavyzdžiui, nitratai, gali pakenkti sveikatai, pvz. mėlyna kūdikio liga, taip pat žinomas kaip infantili methemoglobinemija (mažas hemoglobino kiekis kraujyje). Ši liga pasikartoja kaimo vietovių šeimose dėl žemės ūkio regiono vandens telkinių užteršimo trąšose esančiu amonio nitratu.
pateikė Laysa Bernardes
Chemijos mokytoja
Šaltinis: Brazilijos mokykla - https://brasilescola.uol.com.br/quimica/nitrato-de-amonio.htm
