Kai liepsna veikia skirtingus elementus, pastebime, kad kiekvienas iš jų skleidžia skirtingą spalvą. Pavyzdžiui, jei sudeginsime stroncį, natrio ir vario druską, pamatysime atitinkamai raudoną, intensyviai geltoną ir žalią spalvas, kaip parodyta šiame paveiksle:

Jei šių liepsnų šviesa patenka į prizmę, a nenutrūkstamas spektras, tai yra, bus pastebėtos tik kelios spalvotos ryškios linijos, įsiterpusios į regionus be šviesos. Kiekvienam elementui turėsime skirtingą spektrą.

Šie spektrų tipai vadinami emisijos spektras, nes juos išdavė tam tikras elementas ir jie naudojami jam identifikuoti.
Tokius spektrus galima gauti naudojant šviesos spindulį, susidariusį elektros iškrovos vamzdyje aukštai temperatūros ir žemo slėgio, kurių sudėtyje yra tam tikrų elementų, pvz., vandenilio, dujų arba iš tauriųjų dujų žemyn:

Perduodant šią elektromagnetinę spinduliuotę (šviesą), gaunamą per prizmę, gaunami kiekvieno iš šių elementų emisijos spektrai.
Anksčiau manyta, kad pasiektas saulės spektras yra ištisinis, tačiau anglų mokslininkas Williamas Hyde'as Wollastonas nustatė, kad dirbant su labai siauru šviesos pluoštu, kurio plyšys apie 0,01 mm, matėsi, kad saulės spektras apima septynias juodas linijas apie tai. Vėliau jaunieji
Josephas Fraunhoferis (1787-1826), naudodamas prizmes ir difrakcines groteles, nustatė, kad Saulės spektre iš tikrųjų yra tūkstančiai uždėtų juodų linijų.Kurį laiką vėliau fizinis Gustavas Robertas Kirchhoffas jis pastebėjo, kad geltonos dėmės, gaunamos natrio spektru, yra lygiai toje pačioje vietoje kaip dvi juodos linijos Saulės spektre. jis ir chemikas Robertas Wilhelmas Bunsenas atliko keletą eksperimentų ir pastebėjo, kad jei baltoji šviesa iš Bunseno degiklio, pavyzdžiui, saulės šviesa, praėjo pro natrio skleidžiamą geltoną šviesą, o spektras būtų sukurtas peržengus prizmę; rezultatas būtų nepertraukiamas saulės spektras, vaivorykštės spalvomis, tačiau juodos linijos (Fraunhoferio vadinamos D linijomis) būtų toje pačioje padėtyje kaip ir geltonos linijos natrio spektre.
Nesustokite dabar... Po reklamos yra daugiau;)
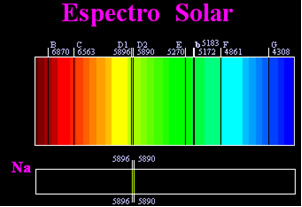
Saulė skleidžia visų spalvų šviesą, nuo raudonos iki violetinės, tačiau eidamos per Žemės atmosferą esančios dujos sugeria Saulės šviesą tiksliai jų skleidžiamomis spalvomis.
Šie spektrų tipai vadinami absorbcijos spektrai.
Remiantis šiais pastebėjimais, Kirchoffas sukūrė tris įstatymai spektroskopijai, kurie yra:
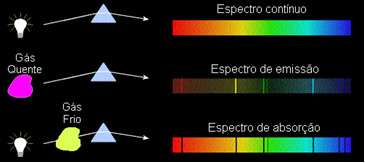
1) Kūnas nepermatomas karštas bet kurioje iš trijų fizinių būsenų skleidžia spektrą nepertraukiamas.
2) dujos skaidrus - kaip ir tauriųjų dujų, kurias matėme aukščiau, gamina a emisijos spektras, su išvaizda linijos ryškus. Šių linijų skaičių ir padėtį nulems dujose esantys cheminiai elementai.
3) Jei a nuolatinis spektras praeina per dujas žemiausioje temperatūroje šaltos dujos sukelia tamsios linijos, tai yra absorbcijos spektras. Taip nutiko saulės spindulių, einančių per natrio dujas, spektrui. Šiuo atveju linijų skaičius ir padėtis absorbcijos spektre taip pat priklauso nuo dujose esančių cheminių elementų.
Jennifer Fogaça
Baigė chemiją
Ar norėtumėte paminėti šį tekstą mokykloje ar akademiniame darbe? Pažvelk:
FOGAÇA, Jennifer Rocha Vargas. „Emisijos ir absorbcijos spektrai ir Kirchhoffo dėsniai“; Brazilijos mokykla. Yra: https://brasilescola.uol.com.br/quimica/espectros-emissao-absorcao-leis-kirchhoff.htm. Žiūrėta 2021 m. Birželio 27 d.


