옥텟 규칙에는 예외가 있기 때문에 분자를 형성 할 때 원자 사이의 올바른 배열을 어떻게 알 수 있습니까?
이는 각 구조의 형식적 하중을 계산하여 수행 할 수 있습니다. 0에 가장 가까운 공식 요금은 실제 존재 확률이 가장 높은 요금입니다. "0에 가장 가깝기"이므로 0이 아니어도됩니다.
공식 청구 공식 (Cfo) é:
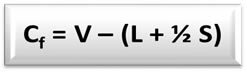
V = 자유 원자의 원자가 전자 수;
L = 구조에서 원자의 분리 된 (비 결합) 쌍에 존재하는 전자의 수;
S = 구조에서 원자가 공유하는 전자의 수.
이것이 어떻게 일어나는지 이해하기 위해 우리가 루이스 전자 구조가 SO 분자에 대해 무엇인지 알고 싶다고 상상해보십시오.2. 원자 사이에는 두 가지 가능한 배열이 있습니다.
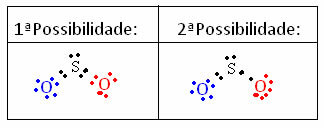
구조에 참여하는 모든 원자의 공식 전하가 계산됩니다. 보기:
첫 번째 가능성 :
황 (S): 산소 (O) 산소 (O)
씨에프 (S) = 6 – (2 + ½ 8) 씨에프 (S) = 6 – (4 + ½ 4) 씨에프 (S) = 6 – (4 + ½ 4)
씨에프 (S) =0 씨에프 (S) =0 씨에프 (S) =0
지금 멈추지 마세요... 광고 후 더 있습니다;)
두 번째 가능성 :
황 (S): 산소 (O) 산소 (O)
씨에프 (S) = 6 – (2 + ½ 6) 씨에프 (S) = 6 – (6 + ½ 2) 씨에프 (S) = 6 – (4 + ½ 4)
씨에프 (S) = +1씨에프 (S) = -1 씨에프 (S) =0
얻은 결과를 바탕으로 첫 번째 구조가 실존 확률이 가장 높은 구조임을 알 수 있습니다. 그래서 우리는 그것이 옥텟 규칙을 따르지 않는다는 것을 압니다. 그러나 유황은 그것의 원자가 껍질을 확장 시켰고, 10 개의 전자로 안정을 유지했습니다.
이 규칙은 올바른 이온 배열을 찾는데도 적용됩니다.
작성자: Jennifer Fogaça
화학 전공
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
FOGAÇA, Jennifer Rocha Vargas. "공식 부하 계산"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/calculo-carga-formal.htm. 2021 년 6 월 28 일 액세스.



