화학을 배우는 모든 사람에게 가장 큰 도전 중 하나는 전자 배포입니다. 이 맥락에서 우리가 제시 할 것은 과학자 Linus Pauling이 제안한 전자 구성과 관련된 연구를 크게 촉진 할 수 있습니다.
각 층 또는 에너지 레벨에 맞는 최대 전자 수는 표를 통해 제공됩니다.
에너지 레벨 레이어 최대 전자 수
첫 번째 K 2
2 차 L 8
3 위 M 18
4 위 N 32
5 ° O 32
6 회 P 18
7 분기 8
하위 레벨 에너지의 증가하는 순서는 대각선 순서의 순서입니다. Linus Pauling 다이어그램은 다음과 같습니다.
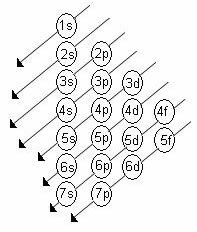
기본 규칙 :
1. 중성 상태에서 원소의 원자 번호 (Z)는 분포 할 전자의 수를 나타냅니다. 이 숫자는 요소 기호의 왼쪽 아래 부분에 표시됩니다.
2. Pauling 다이어그램을 사용하여 증가하는 에너지 순서 (화살표 방향으로 향함)를 고려하여 전자를 위에서 아래로 분배하기 시작합니다.
3. 하위 레벨을 최대 전자 레벨로 채 웁니다. 주어진 하위 레벨이 6 개의 전자 만 보유하고 있다면 그 양을 초과하지 마십시오.
4. 각 하위 수준에서 전자를 더하여 전자 수를 확인합니다.
실행 해보자?
철 원자 (Z = 26)의 전자를 분배합니다.
원자 번호가 26이면 정상적인 철 원자에 26 개의 전자가 있음을 의미합니다. Pauling 다이어그램을 적용하면 다음과 같은 결과를 얻을 수 있습니다.

리리아 알베스
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/regras-distribuicao-eletronica.htm
