뿐만 아니라 사이클란, 알켄, 알킨, 무엇보다도 알카디 엔 또한 부름을 겪는다 부가 반응. 에 대한 텍스트에서 디엔의 반응, 첨가 반응은 작업중인 디엔의 유형에 따라 달라집니다. 디엔은 크게 다음과 같이 분류 할 수 있습니다.
응축 또는 축적 (두 복식 사이에 단일 결합 없음);
예: H2C = CH-CH3
공액 또는 교대 (두 복식 사이의 단일 결합 만);
예: H2C = CH-CH = CH2
외딴 (두 복식 사이에 적어도 두 개의 단일 결합).
예: H2C = CH-CH2-CH2-CH = CH2
Diels-Alder 반응 2 명의 독일 화학자 Otto Paul Hermann Diels와 Kurt Alder에 의해 1928 년에 개발되었습니다. 이것은 유기 화학 내에서 다음과 같은 매우 중요한 반응입니다.
디엔 탄화수소 식별;
포화 고리 형 탄화수소를 얻다 (바람직하게는 시클로 헥산).
이 유기 반응은 알카디 엔 또는 공액 또는 교대 디엔 그리고 불린다 추가 1.4. 더 간단한 방법으로 1,4 첨가를 관찰 할 수있는 화합물은 아래와 같이 but-1,3-diene입니다.
H2C = CH-CH = CH2
노트:이 화합물에서 우리는 공명 현상, 두 파이 결합의 전자가 사슬을 통해 이동합니다. 한쌍 파이 전자 체인의 중앙 영역을 차지하기 시작합니다 (탄소 2와 3 사이), 다른 파이 결합의 전자는 끝 탄소 중 하나로 이동합니다. 따라서 우리는 탄소 1과 4에 결합 부위가 있고 탄소 2와 3 사이에 이중이 있습니다.

but-2,3-diene 구조의 공명
에서 Diels-Alder 반응, 시약 중 하나는 공액 디엔이고 다른 하나는 존재할 수있는 유기 화합물입니다. 전화 탄소 원자 사이에 두 배. 아래는 Diels-Alder 반응 but-2,3-diene과 propene 사이 :
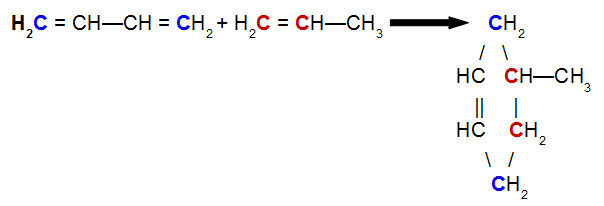
but-2,3-diene과 propene의 Diels-Alder 반응 방정식
위의 방정식을 분석하면 but-2,3-diene 결합의 탄소 1과 4 (둘 다 파란색) 프로 펜의 탄소 1과 2 (모두 빨간색)에 각각 연결되어 분 지형 사이클론을 생성합니다. 4- 메틸-시클로 헥센. 이는 탄소 2와 3 사이의 파이 결합을 이동시키는 but-2,3- 디엔 분자의 공명과 프로 펜의 탄소 1과 2 사이의 파이 결합의 파손 때문입니다.
OBS.² : 공액 알카 디엔과 반응하는 화합물에 관계없이 사슬의 탄소 원자 사이에서만 파이 결합이 끊어진다는 점을 강조하는 것이 중요합니다. 구조에 탄소 이외의 원자 사이에 파이 결합이 있으면 깨지지 않습니다. 아래는 다음과 같이 반응 할 수있는 구조의 예입니다. 알카디 엔 안에 Diels-Alder 반응, 이중 결합의 탄소 (파란색) 사이의 파이 결합이 끊어집니다.
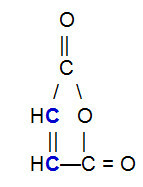
말레 산 무수물의 구조식
나로. Diogo Lopes Dias
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/reacoes-diels-alder.htm