일부 화합물은 안정성을 달성하기 위해 원자가 쉘에 8 개의 전자를 가질 필요가 없으므로 옥텟 규칙의 예외로 간주됩니다. 이제 일부 요소가 마지막 껍질에서 전자 옥텟을 갖는 의무를 벗어나는 이유를 알아보십시오.
베릴륨 (있다)
이것은 두 개의 단일 결합을 가진 화합물을 형성 할 수 있기 때문에 옥텟 규칙의 예외입니다. 
수소 (H)는 결합을 만들기 위해 두 개의 전자를 포기해야하기 때문에 (H-음-H), 베릴륨 (Be) 원자는 전자를 공유하고 안정성을 달성합니다.
알류미늄 (알)
이것은 원자가 쉘에서 6 개의 전자로 안정성을 달성하기 때문에 Octet Rule의 예외입니다. 알루미늄 원자는 전자를 제공하는 경향이 있으므로 다른 원자와 세 개의 단일 결합을 형성 할 수 있습니다. 
이 경우 알루미늄 (Al)은 3 개의 불소 (F) 원자와 3 개의 결합을 형성했습니다.
붕소 (비)
그것은 세 개의 단일 결합으로 분자 물질을 형성합니다. 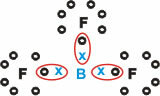
붕소 (B)는 원자가 쉘에 8 개의 전자를 필요로하는 옥텟 규칙을 준수하는 불소 (F) 원자에 전자를 기부하는 경향이 있습니다. 붕소가 전자를 포기함에 따라 불소는 형성된 옥텟과 함께 안정화됩니다.
리리아 알베스
화학 전공
브라질 학교 팀
더보기!
옥텟 이론
일반 화학 - 화학 - 브라질 학교
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm

