그만큼 용해도 또는 용해도 계수, 그것은 실험실에서 항상 실제로 결정되는 물질의 물리적 특성입니다. 소재가 불렀던 용량과 관련이 있습니다. 용질, 다른 사람에 의해 해산 될 선물, 용제.
용해도의 경우 용질은 다음과 같이 분류 할 수 있습니다.
용해성 : 용매에 용해되는 것. 예를 들어 염화나트륨 (용질)은 물 (용매)에 용해됩니다.
약간 용해성 : 용매에 용해하기 어려운 것. 수산화칼슘 [Ca (OH)]의 경우입니다.2] (용질) 물에;
불용성 : 그것들은 용매에 용해되지 않습니다. 예를 들어 모래 (용질)는 물에 녹지 않습니다.
그만큼 용해도 준비와 매우 관련이 있습니다. 솔루션 (균질 혼합물), 용액을 얻기 위해서는 사용 된 용질이 용매에 용해되는 것이 필수적이기 때문입니다.
용해도에 영향을 미치는 요인
용질이 용제에 용해되는 경우에도 용질의 용해 능력에 영향을 미칠 수있는 몇 가지 요인이 있습니다. 그들은 :
a) 용질과 용제의 양과의 관계
용매는 항상 용해 할 수있는 용질의 한계가 있습니다. 용질의 양을 유지하면서 용제의 양을 늘리면 사용 된 용질이 모두 용해되는 경향이 있습니다.
비) 온도
온도는 주어진 용질에 대한 용매의 용해도를 변경할 수있는 유일한 물리적 요인입니다. 이 수정은 아래에서 볼 수 있듯이 용질의 특성에 따라 다릅니다.
흡열 용질: 용매가 실온보다 높은 온도에있는 한 더 큰 질량을 용해시킬 수있는 것입니다. 용매가 뜨거울수록 더 많은 용질이 용해됩니다.
예: 물이 뜨거울 때 더 많은 양의 분쇄 커피를 녹일 수 있습니다.
발열 성 용질 : 용매가 실온보다 낮은 온도에있는 한 더 큰 질량을 용해시킬 수있는 것입니다. 용매가 차가울수록 더 많은 용질이 용해됩니다.
예: 탄산 음료가 차가울 때 더 많은 양의 이산화탄소를 녹일 수 있습니다.
용해도를 결정하는 방법
용해도는 실험적인 방법으로 결정된 속성이므로 일반적으로 재료는 이미 가장 다른 용매에서 용해도를 평가했습니다. 따라서 다음과 같이 특정 용매에서 용질의 용해도에 액세스 할 수 있습니다.
a) 테이블 분석
종종 학생은 테이블 해석에서 용해도를 발견 할 수 있습니다. 다음 예를 참조하십시오.
예: (UEPG-적용됨) 아래 표는 Li 염의 용해도를 보여줍니다2CO3 100g의 물에.

표는 Li의 그램 단위의 질량 값을 나타냅니다.2CO3 0에서 100g의 물에 녹일 수 있습니다. 영형C에서 50 영형씨. 물이 뜨거울수록 Li가 적다는 것을 알 수 있습니다.2CO3 녹는다. 따라서 Li2CO3 발열 성 용질 (물이 차가울 경우 더 많이 용해 됨)입니다.
b) 그래프 분석
용해도는 그래프를 해석하여 평가할 수 있습니다. 이렇게하려면 간단히 온도를 결정하고 곡선으로 전환 한 다음 용해 될 용질의 그램 단위 질량 인 y 축으로 곡선을 돌리면됩니다.
예: (UFTM-적응) 그래프는 AX 염의 용해도 곡선을 보여줍니다.2.
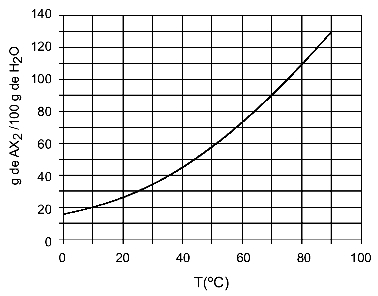
그래프는 y 축에서 물 (용매)의 양이 100g임을 나타냅니다. 용질 AX 용2, 다음 온도에서 물의 양을 결정합니다.
30영형씨: 온도 30을 켜면영형C를 곡선으로, 그리고 곡선을 y 축으로, 이 온도에서 100g의 물이 약 35g의 용질 AX를 용해시킬 수 있습니다.2.
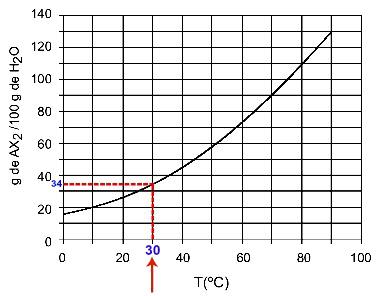
AX 용해도 결정2 30시에영형씨
40영형씨: 온도 40을 켜면영형C를 곡선으로, 곡선을 y 축으로, 이 온도에서 100g의 물은 약 45g의 용질 AX를 용해시킬 수 있습니다.2.
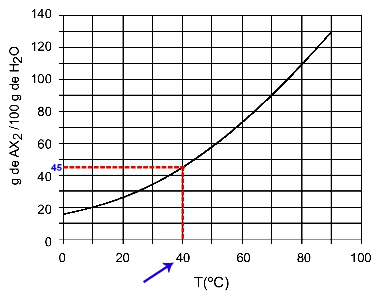
AX 용해도 결정2 40시에영형씨
온도가 상승 할 때마다 용질의 용질의 용해 량이 더 많기 때문에 AX는2 흡열 용질입니다.
c) 텍스트 해석
다음 예를 참조하십시오.
예: (PUC-MG) 특정 물질은 다른 물질과 균질 한 혼합물을 형성 할 수 있습니다. 가장 많은 양의 물질을 용매라고하고 가장 적은 양의 물질을 용질이라고합니다. 염화나트륨 (NaCl)은 물과 균질 한 용액을 형성하며, 물 100g에 NaCl 36g을 20ºC에서 용해시킬 수 있습니다.
본문은 만약 우리가 20의 온도에서 100g의 물 (용제)을 가지고 있다면 영형C, 최대 36g의 NaCl을 용해시킬 수 있습니다.
나로. Diogo Lopes Dias
출처: 브라질 학교- https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-solubilidade.htm



