그만큼 옥텟 이론 화학 원소의 원자가 안정되기 위해서는 희가스의 전자적 구성을 얻어야하며 즉, 원자가 쉘에 8 개의 전자가 있거나 원자에 첫 번째 전자 쉘만있는 경우 2 개의 전자가 있어야합니다. (케이).
베릴륨의 원자 번호는 4입니다. 따라서 원자는 4 개의 전자를 가지며 기저 상태에서의 전자 분포는 다음과 같이 지정됩니다.

베릴륨 전자 구성
이것은 베릴륨이 2A 계열 (알칼리 토금속)의 마지막 껍질에 2 개의 전자를 가지고 있음을 의미합니다. 따라서, 그것은이 두 전자를 기증하는 경향을 가질 것이고, 2+ 전하를 얻는 것, 즉 이온 결합을 형성하는 경향을 가질 것입니다.
그러나 베릴륨 원자는 아래에 형성된 화합물에서 볼 수 있듯이 베릴륨 수 소화물 (BeH2):
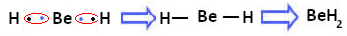
베릴륨과 수소의 공유 결합 형성
이 경우 베릴륨은 원자가 쉘에 전자가 8 개 미만인 상태에서 안정적입니다. 수소 원자처럼 전자를 공유합니다. 이제 마지막에 4 개의 전자가 있습니다. 층. 그러므로 그것은 옥텟 규칙에 대한 예외.
그러나 공유 결합은 일반적으로 요소가 불완전한 궤도를 가지고 있기 때문에 발생합니다. 예를 들어, 아래와 같이 수소는 불완전한 궤도를 가지므로 하나의 공유 결합 만 만듭니다. 산소는 두 개의 불완전한 궤도를 가지며 두 개의 공유 결합을 만듭니다. 차례로 질소는 3 개의 불완전한 궤도를 가지며 결과적으로 3 개의 공유 결합을 만듭니다.
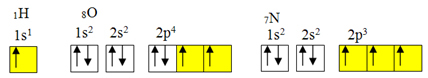
수소, 산소 및 질소의 전자 분포
그러나 이미 표시된 것처럼 베릴륨에는 불완전한 궤도가 없습니다.
그렇다면 공유 결합을 만드는 이유는 무엇입니까?
설명은 혼성화 이론, 즉 궤도의 전자가 에너지를 받으면 가장 바깥 쪽의 빈 궤도로 "점프"합니다. 여기 상태를 유지하여 불완전한 원자 궤도의 융합 또는 혼합이 발생합니다. 생성 하이브리드 궤도 서로 동일하고 원래의 순수 궤도와는 다릅니다.
예를 들어, 베릴륨의 경우 하위 수준 2의 전자가 에너지를 받고 비어있는 하위 수준 2p 궤도로 전달됩니다.

하이브리드 궤도 형성을위한 베릴륨 여기 상태
이런 식으로 베릴륨은 두 개의 불완전한 궤도를 가지며 두 개의 공유 결합을 만들 수 있습니다.
하나의 궤도는 "s"하위 수준에 있고 다른 하나는 "p"에 있으므로 베릴륨이 수행하는 결합은 달라야합니다. 그러나 이것은 일어나는 현상이 아닙니다. 이종 교잡, 형성된 이러한 불완전한 궤도가 혼합되어 잡종 또는 혼성화, 서로 동일합니다. 더욱이, 이 두 가지 하이브리드 궤도는 "s"궤도와 "p"궤도에서 나왔기 때문에이 하이브리드 화는 sp:

베릴륨 sp 혼성화 형성
하이브리드 궤도가 동일하기 때문에 베릴륨이 수소 원자와 만드는 공유 결합도 동일합니다.

하이브리드 베릴륨 궤도와 수소 궤도의 상호 침투
그런 다음 s-sp (σ) 유형의 시그마 결합 두 개를 만듭니다.s-sp).
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/hibridizacao-berilio.htm

