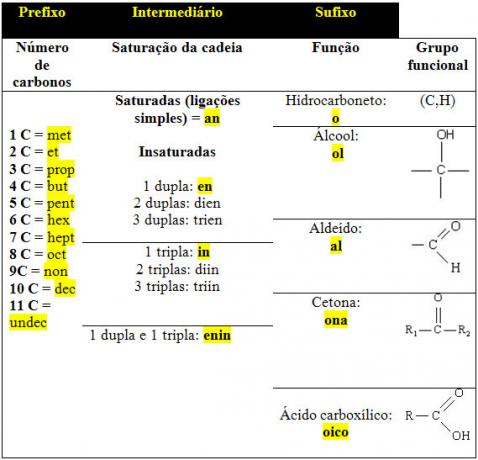
구조식은 구조, 즉 화학 원소를 구성하는 원자의 배열과 그 사이의 연결을 나타내는 체계입니다. 평면, 응축 또는 전자 등 다양한 방식으로 표현할 수 있습니다.
사용되는 구조를 조절하는 요소 중 원자가 껍질의 전자 수가 그중 하나입니다.
플랫 공식
플랫 공식은 대시를 사용하여 공유 결합을 나타내며, 단일, 이중 또는 삼중 일 수 있으며 다음과 같은 방식으로 표현됩니다.
– 간단한 연결 (2 개의 전자가 공유되는 경우)
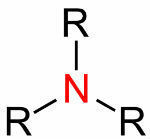
= 이중 결합 (4 개의 전자가 공유 될 때)
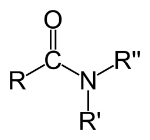
≡ 트리플 링크 (6 개의 전자가 공유 될 때)
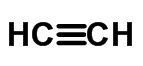
요약 또는 단순화 된 공식
축합 구조식에서 결합은 표시되지 않습니다.
표현에서 각 요소의 원자 수는 축약 된 방식으로 표시됩니다.
H3C CH2 CH2 CH3
선형 요약 공식
선형 축약 공식은 지그재그 선을 사용하며 정점에서 탄소가 표시됩니다.
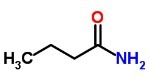
전자 또는 루이스 공식
Lewis 공식이라고도하는 전자 공식은 점으로 표시됩니다.
이러한 점을 통해 원자가 층에 존재하는 전자의 양이 표시됩니다.
H: H
그리고 분자식?
그만큼 분자식, 구조를 참조하지 않고, 구성 요소의 수를 나타냅니다. 분자. 각 원소에 존재하는 원자의 수와 그 비율을 나타내는 것 외에도.
최소 또는 경험적 공식과 백분율 또는 센티 멀 공식을 통해 얻을 수 있습니다.
너무 읽기 이성질체 과 발렌시아 층.
해결 된 연습
1. (Vunesp-2000) 구조식을 작성하고 공식 이름을 지정하십시오.
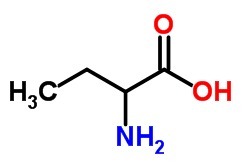
a) 총 7 개의 탄소 원자를 갖는 포화 분 지형 탄소 사슬 케톤.
b) 4 개의 탄소 원자를 가진 아미노산.
그만큼)

비)
2. (FGV-2005) 아스파탐은 1965 년 부주의 한 화학자에 의해 우연히 발견 된 인공 감미료로, 더러운 손가락을 핥고 달콤하다고 느꼈습니다.
이러한 비위생적 습관은 권장되지 않습니다. 소량의 많은 물질이 매우 독성이 있기 때문입니다.
아스파탐의 구조식은 다음과 같습니다.

아스파탐의 구조식에서 보면
a) 분자 당 13 개의 탄소 원자.
b) 1 개의 에테르 작용기.
c) 1 개의 디 펩티드
d) 2 개의 3 차 탄소 원자
e) 단 1 개의 비대칭 탄소 원자.
대안 c: 1 개의 디 펩티드
지식을 계속 테스트하려면 다음 연습 목록도 참조하십시오.
- 탄화수소에 대한 연습
- 유기 화학 연습
- 편평한 이성질체에 대한 연습