할로겐화물은 하나 이상의 할로겐 원자를 갖는 유기 화합물입니다. – 즉, 주기율표 17 또는 VII 계열의 화학 원소 (F, Cl, Br, I 또는 일반적으로: X) – 탄화수소에서 파생 된 그룹에 부착.
RX (여기서 X = F, Cl, Br 또는 I)
일부 할로겐화물은 다음과 같습니다.

할로겐과 탄소 사이의 결합 에너지가 요오드의 방향에서 불소로 증가하기 때문에 요오드는 가장 반응성이 높고 불소는 가장 적게 반응합니다.
또 다른 요점은 반응성도 이러한 의미에서 증가한다는 것입니다.

따라서 이러한 반응성은 유기 할로겐화물에 연결된 탄소에 의해 획득되는 특성으로 인해 3 차 할로겐화 탄소에서 더 쉽게 발생합니다.

따라서 알코올을 형성 할 OH와 같은 치환기는 양의 특성 (1+)을 갖는 3 차 탄소에 더 강하게 끌리고 치환이 더 쉽습니다.
할로겐화물은 실제로 다른 모든 유기 기능 (알코올, 에테르, 알킨, 시안화물 또는 니트릴, 아민 등)을 얻을 수있는 반응을 겪을 수 있습니다. 그러나 할로겐화물은 매우 고가의 화합물이므로 실제로는 불가능합니다.
예를 들어 알코올을 생산하기 위해 할로겐화물은 수성 매질에서 수산화 나트륨과 같은 강염기와 반응합니다. 에틸 클로라이드 (클로로 에탄) 에탄올의 알칼리 가수 분해로부터 형성되는 아래의 예를 보겠습니다.
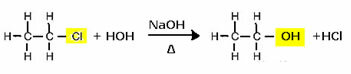
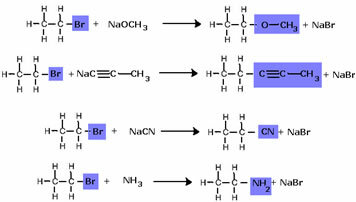
할로겐화물 그룹은 기능성 알코올 그룹 인 OH로 대체되었습니다. 다른 그룹의 형성에도 동일한 계획이 적용되어 시약 만 구별됩니다.
작성자: Jennifer Fogaça
화학 전공
브라질 학교 팀
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/reacoes-substituicao-haletos-organicos.htm
