탄소 사슬은 유기 화합물의 구조를 나타냅니다.
그들은 탄소 원자의 결합에서 형성되기 때문에 그 이름을 얻습니다.
사슬에는 여러 유형이 있으며 탄소 원자의 위치, 그 사이의 결합, 수소 원자 또는 다른 화합물 사이의 결합에 따라 분류가 이루어집니다.
분류
탄소 사슬 분류 기준은 다음과 같습니다.
- 체인 닫기 여부
- 헤테로 원자가 있거나없는 원자 유형 (탄소 또는 수소가 아닌 원자)
- 사슬 원자의 조직
- 원자 사이에 형성된 결합
개방형, 폐쇄 형 또는 혼합형 일 수 있습니다.
1. 오픈 체인
비 환식 및 지방족이라고도합니다. 이 유형의 사슬에서 탄소 원자는 연결되어 끝이 자유 롭습니다.
일반, 직선 또는 선형 개방 체인 :
선형 개방 체인에서는 가지가 형성되지 않습니다.
개방형 분기 체인 :
개방형 분기 체인에는 분기가 있습니다.
개방형 균질 체인 :
동종 사슬에는 탄소 원자가 하나만 있습니다.
그들은 헤테로 원자가 없습니다. 즉 사슬에 탄소 또는 수소 이외의 원자가 없습니다.
이기종 오픈 체인 :
이종 사슬은 사슬을 따라 탄소 또는 수소 이외의 원자가 하나 이상 있습니다.
포화 오픈 체인 :
포화 사슬에서 탄소 원자는 단일 결합으로 함께 연결됩니다. 이 사슬의 탄소를 포화라고합니다.
불포화 오픈 체인 :
이들은 이중에서 삼중 결합으로 연결된 적어도 두 개의 탄소 원자를 가진 사슬입니다. 이 결합에서 탄소를 불포화라고합니다.
2. 닫힌 사슬
폐쇄 또는 순환 사슬은 서로 연결되어 순환을 형성합니다.
방향족 또는 지환 족일 수 있습니다. 지환 족인 경우 동종 고리, 복소 고리, 포화 또는 불포화로 추가로 분류됩니다.
닫힌 방향족 사슬 :
폐쇄 방향족 사슬은 다음과 같이 분류됩니다.
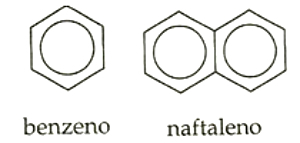
- 단핵: 벤젠과 같은 방향족 고리가 하나만있는 경우.
- 다핵: 나프탈렌과 같은 하나 이상의 방향족 고리가있을 때.
닫힌 지환 족 사슬 :
닫힌 지환 족 사슬은 방향족 고리를 나타내지 않습니다. 그들은 포화와 불포화로 나뉩니다.
불포화 지환 식 폐쇄 사슬은 다음과 같이 나뉩니다.
- 동종의:이 사슬의 고리는 탄소 원자에 의해서만 형성됩니다.
- 이기종: 이들은 이종 원자를 가진 사슬입니다.
포화 폐쇄 사슬 :
포화 사슬에서 모든 탄소 원자는 단일 결합만을 만듭니다.
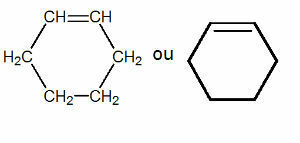
불포화 폐쇄 사슬 :
불포화 사슬에는 원자 사이에 이중 결합이 있습니다.

3. 혼합 체인
혼합 사슬에서 탄소는 함께 결합하고 닫힌 사슬과 마찬가지로 사슬에서 순환을 형성합니다.

읽기 :
- 방향족 탄화수소
- 탄화수소의 명명법
- 유기 화학
- 탄소
체인 탄소 분류
탄소는 체인 내 위치에 따라 다음과 같이 분류 될 수도 있습니다.
1 차 탄소: 사슬의 끝에있는 원자이며 다른 원자에만 결합합니다.

2 차 탄소: 사슬에서 다른 두 개의 탄소 원자에 결합하는 탄소입니다.
3 차 탄소: 탄소가 다른 세 개의 탄소 원자와 결합 할 때.

4 차 탄소: 탄소가 4 개의 다른 탄소 원자에 결합 된 것처럼 보일 때.

읽기 :
- 벤젠
- 탄화수소
- 유기 화합물
- 유기 화학 연습
- 유기적 기능에 대한 연습