유기 화합물은 분자입니다. 즉, 원자는 서로 공유 결합을 가지고 있습니다. 단일, 이중 또는 삼중 일 수있는 탄소 사이의 결합을 분석 할 때 비극성 결합, 원자간에 전기 음성도에 차이가 없기 때문입니다. 요소.
또한 수소와 탄소는 전기 음성도 차이가 매우 작기 때문에 이들 사이의 결합도 비극성입니다.
비극성 연결 :
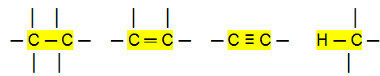
이를 통해 우리는 탄화수소 (탄소와 수소 원자 만있는 유기 화합물) 비극성 분자. 이러한 화합물에서 분자간 상호 작용은 유도 된 쌍극자 유형으로 존재하는 가장 약한 유형입니다.
약하기 때문에 이러한 상호 작용은 깨지기 쉽습니다. 이것 때문에, 탄화수소의 끓는점과 녹는 점은 다른 기능보다 낮습니다.

탄화수소 비교, 몰 질량도 증가함에 따라 끓는점이 증가합니다.
예를 들어, 에탄과 부탄은 모두 알칸입니다. 실험적으로 결정된 각 비등점을 참조하십시오.
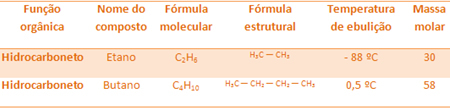
부탄의 끓는점은 몰 질량이 더 높기 때문에 에탄의 끓는점보다 훨씬 높습니다.
이제 우리가 같은 몰 질량 (이성체)을 가지고 있지만 탄소 사슬의 종류가 다른 탄화수소를 비교할 때 우리는 가지 수가 많을수록 끓는 온도는 낮아집니다, 분자의 구조가 더 조밀 해지기 때문에, 즉 표면이 감소합니다.
아래의 모든 알칸은 동일한 분자식 C를 갖습니다.5H12, 그러나 끓는 온도는 다릅니다.
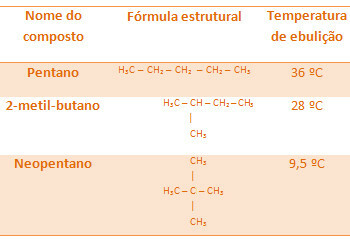
네오 펜탄의 끓는 온도는 가지가 많기 때문에 가장 낮습니다.
다른 유기 기능은 하나 이상의 수소를 다른 원소의 원자 또는 원자 그룹으로 대체하여 탄화수소에서 파생 된 것이라고 생각할 수 있습니다. 일반적으로 다른 유기 기능은 탄소보다 전기 음성 원소 인 산소 또는 질소를 가지고 있습니다. 그들은 탄소와 공유되는 전자 쌍을 더 강하게 끌어 당겨 분자를 극성으로 만듭니다.
극 연결 :
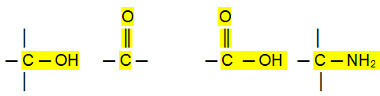
알데히드, 케톤 및 유기 할로겐화물은 끓는점이 분자간 상호 작용이 영구 쌍극자이기 때문에 탄화수소 유도 쌍극자.
반면에 알코올, 카르 복실 산 및 아민은 분자간 상호 작용의 가장 강렬한 유형 인 수소 결합을 수행하기 때문에 끓는 온도가 훨씬 더 높습니다.
이러한 모든 기능의 화합물에서 탄화수소에 대해 본 것과 동일하게 적용됩니다.

작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/polaridade-temperatura-ebulicao-dos-compostos-organicos.htm

