균형이 잡힌 가역적 반응은 균형이 자체적으로 변하지 않기 때문에 외부 변화가있는 경우에만 균형이 이동됩니다.
이러한 변화 중 하나는 시약 또는 제품을 제거하거나 추가하는 농도 변화입니다.
예를 살펴 보겠습니다.
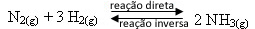
- 시약 추가 :
평형에 더 많은 수소 가스 또는 더 많은 질소 가스를 추가하면 반응물의 농도가 증가하고 그에 따라 분자 사이의 효과적인 충격도 상승하여 직접적인 암모니아 형성 반응의 발달 속도가 증가합니다. (NH3 (g)).
이것은 시약을 추가하면 균형이 오른쪽으로 이동하여 제품이 형성됨을 의미합니다.

이것은 르 샤 틀리에의 원리 그것은 말한다 평형 상태에있는 시스템에서 약간의 장애가 발생하면이 장애를 취소하는 방향으로 이동하여 새로운 평형에 적응하려고합니다.
위의 경우 시간이 지남에 따라 암모니아의 양이 증가하여 다시 평형에 도달하게됩니다. 따라서 제품과 시약의 농도 사이의 비율은 일정하게 유지됩니다. 즉, 평형 상수 Kc의 값은 동일하게 유지됩니다.
Kc = __ [NH3]2__↑
[엔2]. [H2]3 ↑
이는 다른 경우에도 발생합니다. 즉, 시약 또는 제품 농도의 변화가 Kc 값을 변경하지 않습니다.
- 제품 추가 :
암모니아를 더 추가하여 농도를 높이면 일부가 가스로 변합니다. 질소와 수소, 형성의 역 반응의 발달 속도를 증가 시약.
즉, 제품을 추가하면 균형이 시약 형성쪽으로 왼쪽으로 이동합니다.
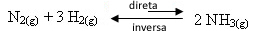
- 시약 제거 :
시약 중 하나 또는 둘 모두를 제거하면 농도가 감소하고 결과적으로 직접 반응의 발달 속도가 감소합니다. 따라서 균형은 왼쪽에있는 더 많은 반응물 형성으로 이동합니다.
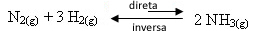
- 제품 철회 :
생성물의 농도를 줄이면 역반응 속도가 감소하여 순 반응 진행 속도가 증가합니다. 이것은 균형이 오른쪽으로 이동한다는 것을 의미합니다.
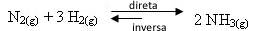
간단히 말해서 다음과 같이 말할 수 있습니다.

강조하는 것이 중요합니다 고체 농도의 변화는 평형을 이동시키지 않습니다.
따라서 아래 반응에서 CO를 제거하거나 추가하면2 (g) 또는 CO(지), 균형에 변화가있을 것입니다. 하지만 C를 줄이거 나 더하면(에스), 화학적 균형으로는 아무 일도 일어나지 않습니다
씨(s) + CO2 (g) ↔ 2 CO(지)
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/variacao-concentracao-deslocamento-equilibrio-quimico.htm
