탄소는 원자 번호 (Z)가 6 인 화학 원소입니다. 즉, 탄소를 형성하는 원자는 핵에 양성자가 6 개 있습니다. 그것의 몰 질량은 12,011 g / mol이며 자연적으로 3 개의 탄소 동위 원소가 발견됩니다. 탄소 -12, 탄소 -13 과 탄소 -14. C-12는 핵에 6 개의 양성자와 6 개의 중성자를 가지고 있으며 가장 풍부합니다.
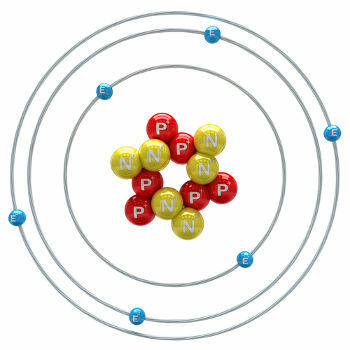
탄소 원자 -12 그림
C-13은 7 개의 중성자를 가지고 있으며 가장 풍부하지 않습니다 (1.01 ~ 1.14 %). C-14에는 8 개의 중성자가 있으며 방사성 원소 이것은 β 입자 (전자)를 방출하며, 우주선 중성자가 대기의 상층에 존재하는 질소 -14를 공격 할 때 지구 성층권에서 형성됩니다. 반감기가 약 5730 년이라는 것을 알고있는 모든 식물과 동물에 통합되어 있으며 100 년에서 40,000 년 사이의 화석 나이를 결정하는 데 사용됩니다. C-14와 데이트 기법에 대한 자세한 내용은 텍스트에서 확인할 수 있습니다. Carbon-14는 무엇입니까?
탄소는 4 가입니다. 즉, 옥텟 규칙을 따르려면 원자가 층 (가장 바깥 쪽 층)에 4 개의 양성자가 더 필요합니다. 따라서 일반적으로 4 개의 공유 결합을 만들어 다른 탄소뿐만 아니라 다른 원소와 4 쌍의 전자를 공유합니다. 이러한 결합은 단일, 이중 또는 삼중 일 수 있으며 수백만 개의 서로 다른 화합물을 형성합니다. 이러한 이유로 화학 영역이 만들어졌고 유기 화학, 다음과 같은 광물 기원의 일부 경우를 제외하고 탄소에서 파생 된 주요 화합물을 연구합니다. 이산화탄소 (CO2), 오 일산화탄소 (CO), 오 탄산 칼슘 (CaCO3), 탄산 수소 나트륨 또는 중탄산 나트륨 (NaHCO3), 다른 사람 사이. 이 화합물은 무기 화학.
탄소는 동소체를 수행하여 단순한 물질, 즉 탄소 원자 사이의 결합에 의해서만 형성되는 물질을 형성합니다. 흑연 (알파 및 베타), 다이아몬드, lonsdaleite (육각 다이아몬드), chaoite, 탄소 (VI) 및 풀러렌 인 탄소 동소체는 최소 7 개 이상 있습니다. 실제로 합성 동소체 형태의 탄소 인 풀러렌에는 여러 유형이 있습니다. 그들은 각 꼭지점에 탄소 원자가있는 다면체 구조를 가지고 있으며 예는
씨60 전화 Buckminsterfullerene, 그 구조는 축구 공처럼 보입니다.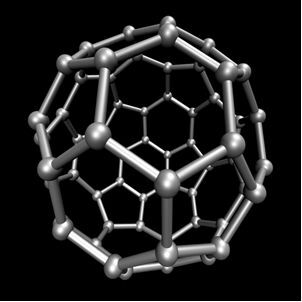
Carbon-60 (벅 민스터 풀러렌)
그러나 이러한 탄소 동소체 중에서 자연적인 것은 두 개뿐입니다. 석묵그것은 ~로부터 다이아몬드. 그것들은 아래 그림과 같이 공간에서 원자의 결정 배열에 의해서만 다르며, 이는 완전히 다른 물리 화학적 특성을 초래합니다. 텍스트 읽기 탄소 동소체 자세한 내용은.

탄소의 두 가지 천연 동소체 형태는 흑연과 다이아몬드입니다.
탄소의 또 다른 합성 동소체 형태는 나노 튜브 (아래 이미지) 의료 진단 및 치료를 포함한 광범위한 생물학적 응용 프로그램이 있습니다.

미세한 탄소 나노 튜브의 그림
그러므로, 탄소는 우리 주변과 우리 안에있는 모든 것에 존재합니다., 그가 작곡하기 때문에 천연 유기 화합물 — 석유, 석탄 및 천연 가스를 포함하는 화석 연료와 에탄올 및 바이오 연료 (농산물 등)와 같은 기타 연료. 모양도 합성 유기 화합물, 직물을 구성하는 합성 섬유, 의약품, 플라스틱 및 고무를 구성하는 폴리머, 살충제, 염료 등. 우리 안에서 동물과 채소는 탄소가 당, 포도당, 셀룰로오스와 같은 탄수화물과 같은 매우 중요한 화합물을 형성합니다. 예를 들어, DNA를 형성하는 단백질과 지질과 함께 적혈구 및 백혈구의 막을 형성합니다.
이 모든 것은 생명 유지를위한 탄소의 중요성을 보여줍니다. 그러나 그것은 또한 강화와 같은 부정적인 측면과 관련이 있습니다. 온실 효과 그리고 그 결과 지구 온난화, 이것은 이러한 문제의 주요 악당이 이산화탄소 화합물 (CO2). 주로이 가스를 방출하는 화석 연료의 대량 연소로 인해 CO의 농도가2 대기에서 증가했습니다. 온실 가스로서 언급 된 문제를 일으 킵니다. 반면에 이산화탄소는 광합성 및 호흡과 같은 중요한 반응에도 존재합니다.
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-carbono.htm