등온 변환에서 부피 및 압력 변화 특정 가스의 일정한 온도; 따라서 등온 이름의 기원 (그리스어에서 유래: iso = 같음; 열 = 열).
과학자 Boyle과 Mariotte는 분리 된 상태에서 유사한 실험을 수행했으며 결과는 압력이 증가함에 따라 가스의 부피가 감소하는 것입니다.
예를 들어 주사기의 플런저를 생각해보십시오. 이 플런저에 외부 압력을 가하면, 즉 압력을 높이면 주사기 내부의 공기량이 감소하고 그 반대의 경우도 마찬가지입니다.
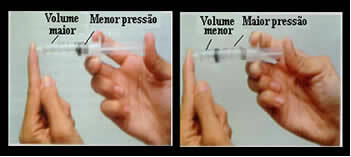
부피와 압력은 반비례합니다. 왼쪽 패널에서는 압력이 작고 공기가 차지하는 부피가 큽니다. 오른쪽에서 주사기 플런저에 더 많은 압력을 가하면 부피가 감소합니다..
이것은 고립 된 경우가 아니라 가스에 대해 일반적인 규칙 성을 가지고 반복되는 것입니다. 따라서이 사실은 다음과 같이 설명 할 수있는 법률 형식으로 명시되었습니다.
| 보일의 법칙 또는 보일-마리오 트의 법칙: 일정한 온도에서 일정한 질량의 가스가 차지하는 부피는 압력에 반비례합니다. |
이것은 우리가 가스의 압력을 두 배로 늘리면 부피가 절반으로 줄어들 것이라는 것을 의미합니다. 그러한 두 양이 반비례 할 때 그 곱은 일정합니다. 따라서 수학적으로이 관계는 다음과 같이 나타낼 수 있습니다.
지금 멈추지 마세요... 광고 후 더 있습니다;)
| P.V = k |
여기서 k = 상수.
따라서 첫 번째 상황에서 특정 가스의 압력 값이 P1이고 해당 부피가 V1 인 경우 다음을 수행해야합니다.
| 피1. V1 = k |
이 압력을 P2로 높이면 볼륨도 V2로 변경되고 다시 다음을 수행해야합니다.
| 피2 . V2 = k |
따라서 우리는 결론에 도달합니다.
| 피1. V1 = P2. V2 |
이 불변성은 아래 표에 주어진 고정 질량을 가진 가스의 압력과 부피의 예에서 볼 수 있습니다.
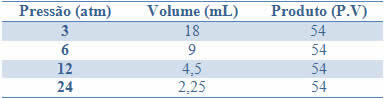
이러한 값을 그래프로 표시하면 곡선이 형성되는 것을 볼 수 있습니다.
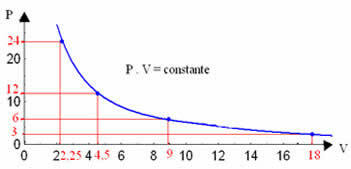
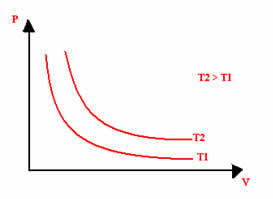
등온 변환의 그래픽 표현은 실험이 수행 된 압력과 부피 및 온도의 값에 관계없이 항상 쌍곡선입니다. 이 쌍곡선은 등온선; 따라서 아래 그래프에서 볼 수 있듯이 온도에 따라 등온선이 달라집니다.
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
FOGAÇA, Jennifer Rocha Vargas. "등온 변환 또는 보일의 법칙"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/transformacao-isotermica-ou-lei-boyle.htm. 2021 년 6 월 27 일 액세스.