용액은 둘 이상의 물질이 균일하게 혼합 된 것입니다.. 예를 들어, 물 (용매)에 용해 된 소금 (용매) 용액.

특히 화학 실험실 및 산업에서는 화학자가 알려진 농도로 용액을 준비해야하기 때문에이 과정이 매우 중요합니다. 또한 실험 활동에서는 농도가 매우 낮은 용액을 사용하므로 농축 용액 샘플을 원하는 농도로 희석합니다.
매일 여러 번 깨닫지 못한 채 용액을 희석하는 과정을 수행합니다. 예를 들어, 소독제와 같은 청소 및 가정용 위생 제품의 포장은 사용하기 전에 희석하도록 권장합니다. 일부 제조업체는 제품 라벨에 1 ~ 3의 비율로 물로 희석, 즉 제품의 각 부분에 물 3 부분을 추가해야한다고 제안합니다. 이는 제품이 고농축되고 튼튼하여 바르게 희석하지 않으면 도포 부위를 손상시킬 수 있기 때문입니다. 반면에, 당신이 그것을 필요 이상으로 희석하면 제품이 원하는 결과를 얻지 못하기 때문에 돈을 잃을 수 있습니다.

또 다른 예는 주스를 만들 때입니다. 많은 농축 주스의 라벨은 주스 한 컵을 희석하거나 물 5 잔과 혼합해야 함을 나타냅니다. 따라서 주스는 "약해져", 즉 덜 농축됩니다.
지금 멈추지 마세요... 광고 후 더 있습니다;)
그런 주스를 물 3L에 희석했다고 상상해보십시오. 초기 주스 농도가 40g / L이면 용매 1 리터당 질량이 40g임을 의미합니다. 그러나 우리는 3L을 가질 것이기 때문에 질량을 3으로 나누고 농도는 용액 1 리터당 약 13, 33g / L 또는 13g이 될 것입니다. 그러나 전체 용액에서 40g 용질의 질량은 여전히 남아 있습니다.
이 새로운 농도의 계산은 다음과 같이 수행 할 수 있습니다.
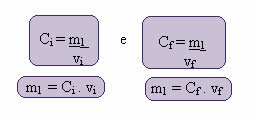
인덱스 i와 f는 각각 초기 값과 최종 값을 나타냅니다. m1의 값은 변경되지 않았으므로 방정식을 동일하게 만들 수 있습니다.
씨나는. V나는 = C에프. V에프
이전 예에 따라 우리가 가진 값을 바꾸면 다음을 참고하십시오.
초기 솔루션 :
씨나는: 40g / L
m1: 40g
V나는: 1L
마지막 해결책:
씨에프: ?
m1: 40g
V에프: 3L
씨나는. V나는 = C에프. V에프
(40g / L). (1L) = C에프. 3L
씨에프 = 40g / L
3
씨에프 = 13.333g / L
몰 농도 (M)와 용질 또는 역가의 질량 백분율 (T)에 대해서도 동일한 추론이 유효합니다.
미디엄나는. V나는 = M에프. V에프 과 티나는. V나는 = T에프. V에프
작성자: Jennifer Fogaça
화학 전공
브라질 학교 팀
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
FOGAÇA, Jennifer Rocha Vargas. "솔루션 희석"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/diluicao-solucoes.htm. 2021 년 6 월 27 일 액세스.