텍스트에 표시된대로 "화학 원소의 전자기 스펙트럼"및"방출 및 흡수 스펙트럼과 Kirchhoff의 법칙”, 각 화학 원소의 불연속 방출 스펙트럼이 다릅니다.

따라서 아래에는 이러한 요소 중 일부의 뚜렷한 스펙트럼이 있습니다.

따라서 덴마크의 물리학자인 Niels Böhr (1885-1962)는 이것이 각 원소의 원자 구조와 관련이있을 수 있음을 깨달았습니다. 그래서 그는 Rutherford의 모델을 보완하는 원자 모델을 제안했지만 원자핵에서 주변 전자의 행동에 초점을 맞추 었습니다.
얼마 전에 Max Planck (1858-1947)는 전자가 양자화, 그들이 마치 작은 에너지 패킷 인 것처럼 특정 양의 에너지를 방출하고 흡수합니다., 그가 전화 얼마예요 (양자, 단수).
따라서 Böhr는 다음을 제안했습니다. 각 원소는 다른 스펙트럼을 가지고 있기 때문에 각 원소는 원소마다 일정하고 다른 에너지의 전자를 원자에 가지고 있습니다.
각 전자는 특정 특정 궤도에만 머물 수 있습니다. 이러한 궤도 각각에서 전자는 일정하고 잘 정의 된 특성 에너지를 갖기 때문입니다. 전자는 각각의 에너지를 가진 에너지 수준 만 차지할 수 있습니다.
전자가 양자화되기 때문에 스펙트럼은 불 연속적입니다.
전자는 에너지를 흡수 할 때만 레벨을 변경할 수 있습니다. 예를 들어 분젠 버너에서 나트륨 염을 태우면 전자에 에너지를 공급하게됩니다. 양자 에너지를 흡수 할 때 전자는 또 다른 에너지 수준으로 점프하여 여기 상태를 유지합니다. 그러나 바닥 상태가 더 안정적이므로이 전자는 흡수 된 에너지를 방출하고 원래 궤도로 돌아갑니다. 빛의 형태로 시각화 할 수있는 전자기파의 형태로이 에너지를 방출합니다. 나트륨의 경우이 빛은 강렬한 노란색입니다. 따라서 이러한 파동이 프리즘을 통과하면 불연속적인 나트륨 스펙트럼이 얻어집니다.
따라서 Böhr에게는 원소의 불연속적인 스펙트럼에 나타난 각 발광 선은 전자가 한 외부 수준에서 핵에 더 가까운 수준으로 돌아 왔을 때 방출되는 에너지를 나타냅니다.
아래 그림은이 문제를 더 잘 이해하는 데 도움이됩니다.
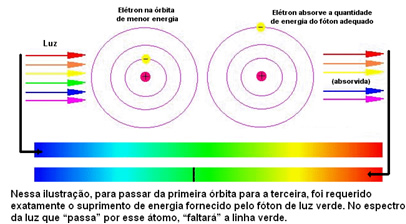
각 요소의 원자는 에너지 층에 해당하는 특정 에너지 값만 허용되므로 각 요소에 대해 다른 스펙트럼이 있습니다.
작성자: Jennifer Fogaça
화학 전공
출처: 브라질 학교- https://brasilescola.uol.com.br/quimica/espectros-eletromagneticos-estrutura-atomo.htm