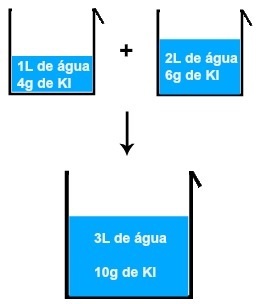
개념을 소개하기 전에 몰 질량과 몰수,이 컨텍스트에서 몇 가지 중요한 정의를 살펴 보겠습니다.
→ 어금니
어금니는 단어에서 유래 분자, 그러나 정확히 분자는 무엇입니까? 화학 결합을 통해 연결된 원자 집합입니다.
→ 분자 질량 (MM)
각 분자를 구성하는 각 원자의 원자 질량의 합으로 분자의 질량을 계산할 수 있습니다. 그 결과를 분자 질량 (MM)이라고합니다.
황화수소의 분자량 (H2S) 예를 들어?
먼저 당신은 무엇을 알아야 원자 질량 주기율표에 의해 주어진 각 원자의 집단.
수소 원자 질량 (H) = 1 a.m.u. (원자 질량 당 단위)
황의 원자 질량 (S) = 32.1 a.u.u.
분자 질량은 원자의 원자 질량의 합입니다.
참고: H 분자의 수소2S의 계수는 2이므로 질량에 2를 곱해야합니다. 계산 :
H의 분자 질량2S = 1 • 2 + 32.1 = 34.1u
(H) + (S) = (H)2에스)
몰 질량과 몰 수
지금 멈추지 마세요... 광고 후 더 있습니다;)
몰 질량과 몰 수는 다음과 관련이 있습니다. 아보가드로 상수 (6.02 x 1023) 다음 개념을 통해 :
''1 몰에 포함 된 기본 개체의 수는 Avogadro 상수에 해당하며 값은 6.02 x 10입니다.23 몰-1.''
따라서 몰 질량은 6.02 x 10의 질량입니다.23 화학 물질이며 g / mol로 표시됩니다.
마인드 맵-Mol
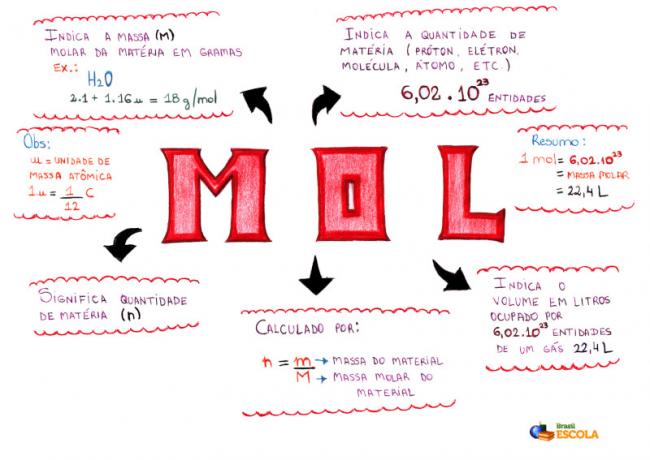
* 마인드 맵을 다운로드하려면 여기를 클릭하세요!
예: H2에스
분자 질량 = 34.1u
몰 질량 (M) = 34.1 g / mol
이것은 34.1 g / mol의 황화수소에서 6.02 x 1023 분자 또는 황화수소 분자 1 몰.
결론
분자 질량과 몰 질량은 동일한 값을 가지며 측정 단위가 다릅니다. 몰 질량은 Avogadro 상수에 의해 주어진 몰 수와 관련이 있습니다.
* 마인드 맵 by Me. Diogo Lopes
리리아 알베스
화학 전공
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
SOUZA, Líria Alves de. "몰 질량 및 몰수"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/massa-molar-numero-mol.htm. 2021 년 6 월 27 일 액세스.