분자는 동일하거나 다른 원소의 원자 그룹입니다. 몇 가지 예를 참조하십시오.
H2영형 -두 개의 다른 원소 (두 개의 수소 원자와 하나의 산소 원자)에 의해 형성된 분자
Cl2– 단 하나의 화학 원소 (2 개의 염소 원자)에 의해 형성된 분자.
에서 분자 분류 할 수 있습니다 극선 또는 무극성 :
비극성: 극이없는 분자 (양극 및 음극);
극선: 극이있는 분자 (양극 및 음극).
이 텍스트에서 우리는 극성 분자. 식별하려면 극성 분자, 아래 제안 된 전략 중 하나를 사용할 수 있습니다.
그만큼) 이온 화합물 (이온 결합에 의해 형성됨)
물질의 출처가 이온 결합 (금속과 비금속 사이) 이온 (양이온과 음이온)에 의해 형성됨을 의미합니다. 따라서이 물질은 자동으로 극성 분자, 이온은 양전하와 음전하를 갖기 때문입니다.
예 :
NaCl (Na는 금속이고 Cl은 비금속 임);
CaO (Ca는 금속이고 O는 비금속 임);
MgS (Mg는 금속, S는 비금속)
비) 분자 화합물 (공유 결합에 의해 형성됨)
화합물이 분자 인 경우 여러 가지 다른 분자가있을 가능성이 있으므로 각 사례를 분석해야합니다. 다음은 극성 분자 화합물의 결정에 도움이 될 수있는 몇 가지 예와 규칙입니다.
- 다른 원소를 가진 이원자 분자
분자 화합물이 두 개의 원자로 구성되어 있고이 두 원자가 서로 다른 원소에서 나온다면 두 원자가 서로 다른 전기 음성도를 가지기 때문에 자동적으로 분자는 극성이됩니다. 예: HBr 및 NO.
- 두 개 이상의 원자를 가진 분자 (동일하거나 다른)
2 개 이상의 원자를 가진 분자에서는 구름의 양을 고려해야합니다. 분자의 중심 원자에 존재하는 결합제와 비 결합제를 원자에 부착 된 동일한 원자의 수와 비교 본부. 결합 구름은 단일 결합 (관련된 각 원자의 원자가 껍질에서 전자 하나), 이중 결합 (2 개 관련된 각 원자의 원자가 껍질에서 전자) 또는 삼중 (각 원자의 원자가 껍질에서 전자 3 개) 뒤얽힌). 비 결합 구름은 결합에 참여하지 않는 원자가 껍질의 전자 쌍입니다.
지금 멈추지 마세요... 광고 후 더 있습니다;)
관측: 주어진 원자의 원자가 껍질에있는 전자의 수를 알려면 주기적 가족을 알면됩니다.

분자가 극성인지 확인하려면 중심 원자에 존재하는 구름의 수가 그 분자에 부착 된 동일한 원자의 수와 다른지 확인하는 것으로 충분합니다. 몇 가지 예를 참조하십시오.
HCN
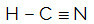
분자의 중심 원자는 탄소이며 두 개의 다른 바인더,두 개의 구속력있는 구름 (단일 및 삼중) 및 비 결합 전자 쌍이 없습니다 (VIA 패밀리에서, 원자가 쉘에 4 개의 전자가 있으며 단일 결합에 하나, 삼중에 3 개를 모두 사용합니다). 이러한 이유로 극성 분자를 형성합니다.
간단히 말해서:
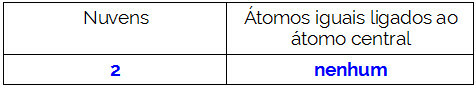
NH3
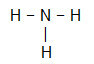
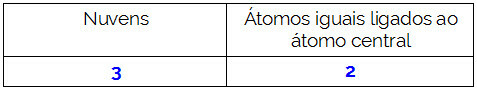
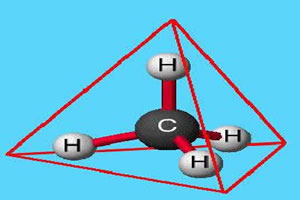
분자의 중심 원자는 질소이며 3 개의 동일한 리간드와 총 네 구름, 3 개의 결합 구름 (3 개의 단일 결합)과 1 개의 비 결합 (VA 패밀리에서 왔으며 5 개의 전자를 가짐) 원자가 층에 있고 각 단일 연결에 하나씩 세 개만 사용하고 두 개는 바인더).
이 때문에 NH의 중심 원자는3 극성 분자를 형성합니다.
요컨대 :

CH2영형
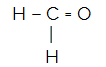
분자의 중심 원자는 탄소이며 두 개의 동일한 리간드와 하나의 다른 리간드세 개의 구속력있는 구름 (단일 결합 2 개 및 이중 결합 1 개), 비 결합 전자 쌍 없음 (VIA 제품군에서 원자가 쉘에 4 개의 전자가 있고 4 개를 사용하고 있습니다. 쌍). 이 때문에 극성 분자를 형성합니다.
간단히 말해서:
나로. Diogo Lopes Dias
이 텍스트를 학교 또는 학업에서 참조 하시겠습니까? 보기:
일, Diogo Lopes. "극 분자"; 브라질 학교. 가능: https://brasilescola.uol.com.br/quimica/moleculas-polares.htm. 2021 년 6 월 28 일 액세스.
이온 화합물, 이온 화합물의 주요 특징, 이온 간 결합, 전자의 확실한 전달, 이온, 음이온 및 양이온, 음이온, 양이온, 이온 결합, 분자 구조 사이의 정전기 인력 그
화학
분자 물질, 끓는점, 접촉면, 끓는점, 분자간 인력, 화학 결합, 분자 화합물, 공유 화학 결합, 이온 결합, 금속 결합, 물리적 상태 나쁜

