ჟანგვის შემცირების რეაქციები, რომლებიც ხდება წყალბადის ზეჟანგის (წყალბადის ზეჟანგის წყალხსნარი - H) არსებობისას2ო2 (aq)) წარმოადგენს განსაკუთრებულ შემთხვევას, რომელიც ცალკე უნდა იქნას გაანალიზებული, ძირითადად მისი ბალანსის გათვალისწინებით. ეს იმიტომ ხდება, რომ წყალბადის ზეჟანგში ჟანგბადებს, რომელთა Nox -1 ტოლია, შეიძლება ან დაჟანგდეს, ან შემცირდეს.
მაგალითად, მოდით განვიხილოთ ორი შემთხვევა, როდესაც იგი იქცევა ჯერ როგორც ჟანგვითი (ამცირებელი) და შემდეგ როგორც შემამცირებელი საშუალება (ჟანგვა):
- ჟანგვის აგენტი: როდესაც წყალბადის ზეჟანგი მცირდება, მოქმედებს როგორც ჟანგვითი აგენტი, ის წარმოქმნის წყალს, როგორც პროდუქტს.
თუ იოდის იონების შემცველ ხსნარს დავუმატებთ წყალბადის ზეჟანგის ხსნარს (I-) მჟავე გარემოში გვექნება:
ჰ2ო2 (aq) + მე-(აქ) + თ+(აქ) თ2ო(1) + მე2 (s)
ნახეთ, რომ წარმოიქმნება წყალი და იოდი. მაგრამ იმის შესამოწმებლად, მოქმედებდა თუ არა წყალბადის ზეჟანგი ჟანგვის შემცველობით და შემცირდა, დააკვირდით დაჟანგვის რიცხვების (NOx) განსაზღვრას: *

წყალბადის ზეჟანგის ჟანგბადის Nox შემცირდა -1-დან -2-მდე, იმის გათვალისწინებით, რომ მან მიიღო 1 ელექტრონი. ამასთან, რადგან წყალბადის ზეჟანგის მოლეკულაში გვაქვს ორი ჟანგბადი (H
2ო2), Nox ვარიაცია ტოლი იქნება 2-ის.ასე რომ, როგორც ეს ნაჩვენებია ტექსტში ”Redox დაბალანსება”, აუცილებელი ნაბიჯი ჟანგვა-შემცირების მეთოდით რეაქციების დასაბალანსებლად არის Nox- ის ვარიაციების მნიშვნელობების ინვერსირება კოეფიციენტებით, ამ შემთხვევაში ასეთია:
* ჰ2ო2 = 2 (oxNox) = 2 2 იქნება I კოეფიციენტი-;
* ᲛᲔ-= OxNox = 1 → 1 იქნება H კოეფიციენტი2ო2.
ამრიგად, ჩვენ გვაქვს:
1 საათი2ო2 (aq) + 2 მე-(აქ) + თ+(აქ) თ2ო(1) + მე2 (s)
სხვა კოეფიციენტების დარტყმა საცდელი ბალანსირებით:
- რადგან 1 წევრში არის ჟანგბადის ორი ატომი, მე -2 წევრის წყლის კოეფიციენტი უნდა იყოს 2. და რადგან 1 წევრში ასევე არის ორი იოდიდის იონი, იოდის კოეფიციენტი მე -2 წევრში იქნება 1. არ უნდა დაგვავიწყდეს, რომ ინდექსი უნდა გავამრავლოთ კოეფიციენტზე, რათა თითოეულ წევრში ვიპოვოთ ატომებისა და იონების სწორი რაოდენობა:
1 საათი2ო2 (aq) + 2 მე-(აქ) + თ+(აქ) → 2 ჰ2ო(1) + 1 მე2 (s)
ნუ გაჩერდები ახლა... რეკლამის შემდეგ მეტია;)
- ახლა მხოლოდ 1-ლი წევრის წყალბადის კატიონის დაბალანსება რჩება და მისი კოეფიციენტი უნდა იყოს 2-ის ტოლი, რადგან მე -2 წევრში მას აქვს 4 წყალბადის და 1-ლი წევრის შემადგენლობაში უკვე ორი:
1 საათი2ო2 (aq) + 2 მე-(აქ) +2 სთ+(აქ) → 2 ჰ2ო(1) + 1 მე2 (s)
- შემცირების აგენტი: როდესაც წყალბადის ზეჟანგი იჟანგება, მოქმედებს როგორც შემამცირებელი საშუალება, წარმოქმნის ჟანგბადს (O2) როგორც პროდუქტი.
წყალბადის ზეჟანგის შემცირების მაგალითია კალიუმის პერმანგანატთან (KMnO) კონტაქტის დროს4). ამ ნივთიერებას აქვს ძალიან დამახასიათებელი იისფერი ფერი, მაგრამ წყალბადის პეროქსიდთან კონტაქტის დროს ხდება უფერო. ეს იმიტომ ხდება, რომ MnO იონში არსებული ყველა მანგანუმი4- მცირდება პერმანგანატის ხსნარი და წარმოიქმნება Mn იონი2+, როგორც ქვემოთაა ნაჩვენები:
+1 -1 +7 -2 +1 0 +2 +1 -2
ჰ2ო2 + MnO4-+ თ+ → The2 + მნ2++ თ2ო
გაანგარიშების Nox, ჩვენ ვხედავთ, რომ ჟანგბადის წყალბადის პეროქსიდი რეალურად იჟანგება და იწვევს მანგანუმის შემცირებას:
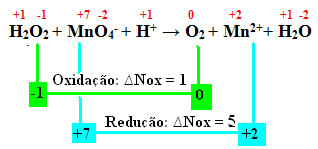
როგორც წინა მაგალითში, ,NO წყალბადის ზეჟანგი ტოლი იქნება 2-ის, რადგან არსებობს ორი ჟანგბადი და თითოეული კარგავს ელექტრონს. ამიტომ, ჩვენ გვაქვს:
* ო2 = 2 (oxNox) = 2 2 იქნება MnO კოეფიციენტი4-;
* MnO4- = OxNox = 5 5 იქნება O კოეფიციენტი2.
და როგორც ყველა ო2 მოდის წყალბადის ზეჟანგიდან, ორ ნივთიერებას აქვს იგივე კოეფიციენტი:
5 ჰ2ო2 + 2MnO4-+ თ+ → 5 ო2 + მნ2++ თ2ო
საცდელი მეთოდით დაბალანსება გვაქვს:
5 საათი2ო2 + 2 MnO4-+ 6 სთ+ → 5 O2 + 2 მილიონი2++ 8 სთ2ო
* ნებისმიერი კითხვისთვის, თუ როგორ გამოვთვალოთ ატომებისა და იონების დაჟანგვის ნომერი (Nox) რეაქციაში, წაიკითხეთ ტექსტი „დაჟანგვის რიცხვის განსაზღვრა (Nox)“.
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია
გსურთ მიუთითოთ ეს ტექსტი სასკოლო ან აკადემიურ ნაშრომში? შეხედე:
FOGAÇA, ჯენიფერ როშა ვარგასი. "ჟანგვის შემცირების რეაქციები წყალბადის ზეჟანგის ჩათვლით"; ბრაზილიის სკოლა. Ხელმისაწვდომია: https://brasilescola.uol.com.br/quimica/reacoes-oxirreducao-envolvendo-agua-oxigenada.htm. წვდომა 2021 წლის 28 ივნისს.


