ოქტეტის თეორია აცხადებს, რომ ქიმიური ელემენტის ატომის სტაბილურობისთვის მან უნდა შეიძინოს კეთილშობილი გაზის ელექტრონული კონფიგურაცია, ანუ მას უნდა ჰქონდეს რვა ელექტრონი ვალენტურ გარსში ან ორი ელექტრონი, თუ ატომს მხოლოდ პირველი ელექტრონული გარსი აქვს. (K)
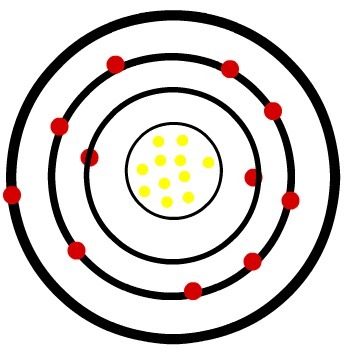
ბერილიუმს აქვს 4-ის ტოლი ატომური რიცხვი. ამიტომ, თქვენს ატომს აქვს 4 ელექტრონი და მის ელექტრონულ განაწილებას საფუძველში მოცემულია:

ბერილიუმის ელექტრონული კონფიგურაცია
ეს ნიშნავს, რომ ბერილიუმს აქვს უკანასკნელი გარსი 2 ელექტრონი, 2A ოჯახიდან (ტუტე მიწის ლითონები). ამრიგად, მას ექნება ამ ორი ელექტრონის გაღების ტენდენცია, მიიღებს მუხტს 2+, ანუ მას აქვს იონური ბმების ფორმირების ტენდენცია.
ამასთან, დაფიქსირებულია, რომ ბერილიუმის ატომები ქმნიან კოვალენტურ კავშირებს, ელექტრონების განაწილებით, როგორც ეს ნაჩვენებია ქვემოთ წარმოქმნილ ნაერთში, ბერილიუმის ჰიდრიდი (BeH2):
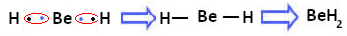
ბერილიუმის კოვალენტური ბმების წარმოქმნა წყალბადთან
გაითვალისწინეთ, რომ ამ შემთხვევაში, ბერილიუმი სტაბილურია და მისი ვალენტური გარსით რვაზე ნაკლები ელექტრონია, რადგან იზიარებენ მის ელექტრონებს, როგორც წყალბადის ატომებს, ახლა მას აქვს ბოლო ოთხი ელექტრონი ფენა. ეს, მაშასადამე, ა
ოქტეტის წესის გამონაკლისი.მაგრამ კოვალენტური კავშირი ჩვეულებრივ ხდება, რადგან ელემენტს არასრული ორბიტალები აქვს. მაგალითად, როგორც ნაჩვენებია ქვემოთ, წყალბადს აქვს არასრული ორბიტალი, ამიტომ ის მხოლოდ ერთ კოვალენტურ კავშირს ქმნის. ჟანგბადს აქვს ორი არასრული ორბიტალი და ქმნის ორ კოვალენტურ ბმას. აზოტს, თავის მხრივ, აქვს სამი არასრული ორბიტალი და, შესაბამისად, ქმნის სამ კოვალენტურ ბმას:
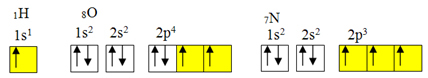
წყალბადის, ჟანგბადის და აზოტის ელექტრონული განაწილება
ამასთან, როგორც უკვე ნაჩვენებია, ბერილიუმს არ აქვს არასრული ორბიტალები.
ნუ გაჩერდები ახლა... რეკლამის შემდეგ მეტია;)
რატომ ქმნის კოვალენტურ კავშირებს?
განმარტება არის ჰიბრიდიზაციის თეორია, რომელიც ამბობს რომ როდესაც ელექტრონი ორბიტალიდან იღებს ენერგიას, ის "ხტება" ყველაზე ცარიელ ორბიტალზე, აღგზნებულ მდგომარეობაში დარჩენა და ამით ხდება არასრული ატომური ორბიტალების შერწყმა ან შერევა, მომტანი ჰიბრიდული ორბიტალები რომლებიც ერთმანეთის ეკვივალენტურია და განსხვავდება ორიგინალური სუფთა ორბიტალებისაგან.
მაგალითად, ბერილიუმის შემთხვევაში, ელექტრონი 2-ე ქვესკნელიდან იღებს ენერგიას და გადადის ქვექვეშა 2p ორბიტალზე, რომელიც ცარიელი იყო:

ბერილიუმ აღფრთოვანებული მდგომარეობა შექმნა ჰიბრიდული ორბიტალები
ამ გზით, ბერილიუმს აქვს ორი არასრული ორბიტალი, რომელსაც შეუძლია შექმნას ორი კოვალენტური ბმა.
გაითვალისწინეთ, რომ ერთი ორბიტალი არის "s" ქვესქვეშეთში, ხოლო მეორე "p", ამიტომ ბერილიუმის შეკავშირებები უნდა იყოს განსხვავებული. ამასთან, ეს არ ხდება, რადგან ფენომენის დროს ჰიბრიდიზაცია, ეს არასრული ორბიტალები, რომლებიც წარმოიქმნება, შეერევა და წარმოქმნის ორ ორბიტალს ე.წ. ჰიბრიდები ან ჰიბრიდიზებული, რომლებიც ერთმანეთის ტოლია. უფრო მეტიც, ვინაიდან ეს ორი ჰიბრიდული ორბიტალი წარმოიშვა "s" ორბიტალიდან და "p" ორბიტალიდან, ჩვენ ვამბობთ, რომ ეს ჰიბრიდიზაცია ტიპისაა სპ:

ბერილიუმის sp ჰიბრიდიზაციის ფორმირება
მას შემდეგ, რაც ჰიბრიდული ორბიტალები იგივეა, კოვალენტური ბმები, რომლებიც ბერილიუმს ქმნის წყალბადის ატომებთან, იგივე იქნება:

ჰიბრიდული ბერილიუმის ორბიტალების ინტერპენერაციები წყალბადის s ორბიტალებთან
გაითვალისწინეთ, რომ შემდეგ ხდება ორი სიგმა ობლიგაციები, რომლებიც s-sp ტიპისაა (σ.)s-sp).
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია