მას შემდეგ, რაც ათასობით ორგანული ნაერთია, იზომერიის ფენომენმა შეიძლება რამდენიმე ფორმა მიიღოს. ამიტომ, იზომერია ძირითადად შეიძლება დაიყოს ორ ტიპად: ბრტყელი ან კონსტიტუციური იზომერია და სივრცის იზომერიზმი ან სტერეოიზომერია. თითოეული აღნიშნული ტიპი შეიძლება დაიყოს, როგორც ნაჩვენებია შემდეგ დიაგრამაზე:
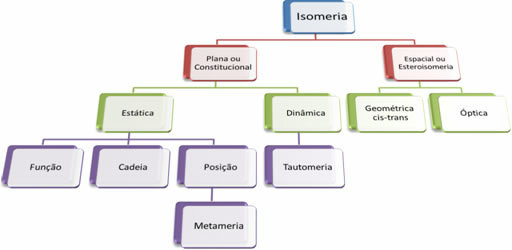
იხილეთ თითოეული შემთხვევა:
1. ბრტყელი ან კონსტიტუციური იზომერია: ამ ტიპის იზომერებს აქვთ იგივე მოლეკულური ფორმულა და გამოირჩევიან ბრტყელი სტრუქტურული ფორმულებით. არსებობს თვითმფრინავის იზომერიის ხუთი შემთხვევა: ფუნქცია, ჯაჭვი, პოზიცია, მეტამერიზმი და ტავტომერია.
1.1.ფუნქციური ან ფუნქციური იზომერია: იზომერებს შორის განსხვავება ფუნქციურ ჯგუფშია.
მაგალითი: მოლეკულური ფორმულა C3ჰ6ო
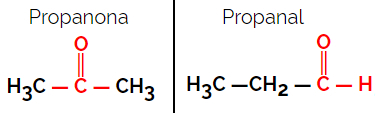
გაითვალისწინეთ, რომ პროპანონი არის კეტონების ჯგუფიდან და პროპანალი არის ალდეჰიდების ჯგუფიდან.
1.2. ჯაჭვის ან ჩონჩხის იზომერები: იზომერებს შორის განსხვავება ჯაჭვის ტიპშია. მაგალითად, ერთი იზომერი არის ღია ჯაჭვი, ხოლო მეორე დახურული, ან ერთი არის ნორმალური, ხოლო მეორე - განშტოებული, ან ერთი არის ერთგვაროვანი და მეორე ჰეტეროგენული.
მაგალითი: მოლეკულური ფორმულა C4ჰ10
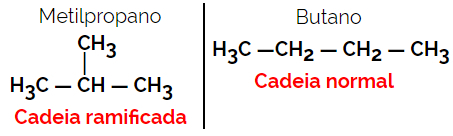
1.3.პოზიციური ან პოზიციური იზომერია: განსხვავება არის გაჯერების, ფუნქციური ჯგუფის, ჰეტეროატომის ან შემცვლელი ნივთიერების პოზიციაში.
მაგალითი: მოლეკულური ფორმულა C4ჰ6

1.4.კომპენსაციის იზომერია ან მეტამერია: ეს არის სპეციალური ტიპის პოზიციური იზომერია, სადაც განსხვავებაა ჰეტეროატომის პოზიცია.
მაგალითი: მოლეკულური ფორმულა C4ჰ10ო
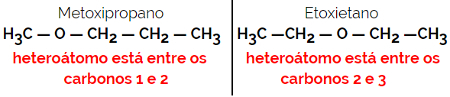
1.5.დინამიური იზომერია ან ტავტომერია: ეს არის სპეციალური ტიპის ფუნქციის იზომერია, რომელშიც იზომერები თანაარსებობენ ხსნარში დინამიურ წონასწორობაში. ტავტომიის ორი ძირითადი ტიპია კეტონსა და ენოლს (კეტოენოლის ბალანსი) და ალდეჰიდსა და ენოლს (ალდოენოლის ბალანსი) შორის.
მაგალითი: მოლეკულური ფორმულა C3ჰ6ო
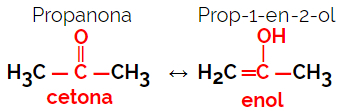
2. კოსმოსური იზომერია ან სტეროიზომერია: ამ შემთხვევაში იზომერებს შორის განსხვავება მხოლოდ მათი ატომების სივრცეში ორიენტაციის საშუალებით შეიძლება ვიზუალიზაცია. არსებობს სტერეოიზომერიის ორი ტიპი: გეომეტრიული იზომერია და ოპტიკური იზომერია.
2.1.გეომეტრიული ან ცის-ტრანს იზომერები: განსხვავება იმაშია, რომ იზომერი სახელად, როგორც დსთ მას აქვს იგივე ნახშირბადის ლიგანდები ორმაგ კავშირში ან ციკლური ნაერთებში სიბრტყის იმავე მხარეს. იზომერული ლიგანდები ტრანს მოპირდაპირე მხარეებზე არიან.
მაგალითი: მოლეკულური ფორმულა C2ჰ2კლ2

ამ ნაერთებს უწოდებენ სტერეოიზომერები.
2.2.ოპტიკური იზომერი: ხდება, როდესაც იზომერებს შეუძლიათ პოლარიზებული სინათლის სხივის გადახრა. თუ იგი პოლარიზებული სინათლის სხივს მარცხნივ დაატრიალებს, ეს ლევოროტარული იზომერია, მაგრამ თუ მარჯვნივ მოხრის, მას მარჯვენა ხელის იზომერი ეწოდება.
მაგალითი:
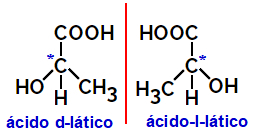
ასიმეტრიული მოლეკულები, როგორიცაა ზემოთ ნაჩვენები, რომლებიც ერთმანეთის სარკისებური გამოსახულებებია და რომლებიც არ არის ზედმეტი, ე.წ. ენანტიომერები.
ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/quimica/tipos-isomeria.htm


