შეგვიძლია აღვნიშნოთ, რომ ყოველთვის, როდესაც ქიმიურ რეაქციაში მონაწილე ერთი ან ყველა რეაქტივის კონცენტრაციას ვზრდით, იზრდება მისი განვითარების სიჩქარე, ანუ რეაქციის სიჩქარე.
პირიქითაც არის მართალი. მაგალითად, ამჟამად გვირჩევენ, რომ ჩვეულებრივი ალკოჰოლის ნაცვლად გამოვიყენოთ ალკოჰოლის გელი, რადგან მისი დაწვის და ამით ავარიების თავიდან აცილების რისკი ნაკლებია. ჩვეულებრივი თხევადი ალკოჰოლი სინამდვილეში არის ალკოჰოლისა და წყლის ნარევი, გელი ალკოჰოლი შეიცავს მცირე რაოდენობით ალკოჰოლს. ამიტომ, როდესაც წვის ერთ-ერთი რეაქტორის კონცენტრაცია მცირდება, ალკოჰოლის შემთხვევაში, რეაქცია მიმდინარეობს უფრო ნელა. მეორეს მხრივ, სუფთა ალკოჰოლი, უფრო სწრაფია წვის რეაქცია.

როგორც ტექსტშია ნათქვამი ქიმიური რეაქციების წარმოქმნის პირობები, რეაქციის ერთ-ერთი პირობაა ეფექტური შეჯახება ნაწილაკებს შორის. ამრიგად, რეაგენტების კონცენტრაციის ზრდა საშუალებას იძლევა უფრო მეტი ნაწილაკები ან მოლეკულები იყოს იგივე სივრცეში. ეს ზრდის მათ შორის შეჯახებების რაოდენობას და ასევე ზრდის ეფექტურ შეჯახების ალბათობას, რაც გამოიწვევს რეაქციას. შედეგი არის ის, რომ რეაქცია უფრო სწრაფად ხდება.
ამის სანახავად, დაფიქრდით შემდეგ მაგალითზე: როდესაც ჩვენ გვწვავს ზურმუხტი და გვინდა, რომ ეს წვა უფრო სწრაფად დამუშავდეს, ვუშვებთ თუ არა ზამბარას? რატომ მუშაობს ეს?
კარგად, ამ წვის რეაქციის ერთ-ერთი რეაქტორი არის ჟანგბადი ჰაერში. როდესაც ჩვენ ვძვრებით, ჰაერის მიმდინარეობა ხსნის ნაცარს, რომელიც იქმნება წვის დროს და ეს ხელს უწყობს ჟანგბადის კონტაქტს ზამბარასთან. ამ გზით, ჩვენ ვზრდით კონტაქტს რეაქტორებს შორის და ვაჩქარებთ წვის რეაქციას.
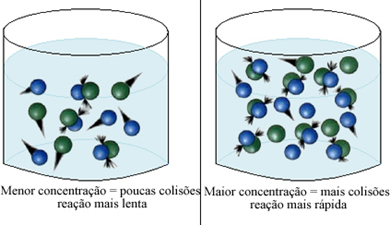
მოკლედ, გვაქვს:

გაზებზე მუშაობისას, რეაქტიული ნივთიერებების კონცენტრაციის გაზრდის ერთი გზაა შეამცირეთ წნევა. როდესაც ამას ვაკეთებთ, ვამცირებთ მოცულობას და, შესაბამისად, იზრდება რეაგენტის კონცენტრაცია.

ჯენიფერ ფოგაჩას მიერ
დაამთავრა ქიმია
წყარო: ბრაზილიის სკოლა - https://brasilescola.uol.com.br/quimica/concentracao-dos-reagentes-velocidade-das-reacoes.htm
