THE ჰასიუმი, სიმბოლო Hs და ატომური ნომერი 108, არის ერთ-ერთი ელემენტი, რომელიც ცნობილია როგორც ტრანსაქტინიდები. ამ ჯგუფის ყველა ელემენტის მსგავსად, ის ბუნებაში არ არის ნაპოვნი, არის სინთეზური, გარდა ამისა, არის რადიოაქტიური და არასტაბილური. მისი სინთეზი მიეკუთვნება ჰელმჰოლცის მძიმე იონების კვლევის ცენტრის (GSI) გერმანულ ლაბორატორიებს, ქალაქ ქ. დარმსტადიუმში, გერმანია, და მისი სახელი ეწოდა გერმანიის შტატის ჰესეს პატივსაცემად, რომელიც მდებარეობს ცენტრალურ რეგიონში. მშობლები.
ჰასიუმი არის უმძიმესი ელემენტი, რომლის თვისებებიც გაანალიზებულია თავად GSI-ის მიერ ჩატარებული ექსპერიმენტებით. შედეგები მნიშვნელოვანი იყო H-ების პოზიციის დასადასტურებლად Პერიოდული ცხრილი, როგორც მსგავსება ამ ელემენტსა და მე-8 ჯგუფის უფრო მსუბუქ ელემენტებს შორის ოსმიუმსა და რუთენიუმს შორის.
წაიკითხეთ ასევე:ბორიუმი — სინთეზური ქიმიური ელემენტი, რომელსაც ნილს ბორის სახელი ეწოდა
ჰასიუმის რეზიუმე
ეს არის სინთეზური ქიმიური ელემენტი, რომელიც მდებარეობს პერიოდული ცხრილის მე-8 ჯგუფში.
იგი სინთეზირებული იყო Gesellschaft für Schwerionenforschung (GSI) მიერ დარმსტადიუმში, გერმანია.
Ეს არის რადიოაქტიური ელემენტი და არასტაბილური.
თეორიული და ექსპერიმენტული მონაცემები ადასტურებს, რომ მისი თვისებები წააგავს მისი ჯგუფის ყველაზე მსუბუქ ელემენტებს.
როგორც ტრანსაქტინიდი, ის არ შეიძლება წარმოიქმნას ფართო მასშტაბით, გარდა რამდენიმე სიჩქარით წარმოებული ატომები.
არ გაჩერდე ახლა... რეკლამის შემდეგ კიდევ არის ;)
ჰასიუმის თვისებები
სიმბოლო: ჰს
ატომური ნომერი: 108
ატომური მასა: 277 წ.
ელექტრონული კონფიგურაცია: [Rn] 7 წმ2 5ფ14 6d6
ყველაზე სტაბილური იზოტოპი: 269Hs (14 მეორე ნახევარგამოყოფის პერიოდი)
ქიმიური სერია: ჯგუფი 8; ტრანსაქტინიდები; სუპერ მძიმე ელემენტები.
ჰასიუმის თვისებები
ჰასიუმი არის ა სინთეზური ელემენტი და ყველაზე მძიმე მე-8 ჯგუფიდან. ითვლება ა ტრანსაქტინიდი, ზუსტად იმიტომ, რომ ის ჩნდება პერიოდულ ცხრილში აქტინიდების სერიის შემდეგ. ყველა ტრანსაქტინიდის მსგავსად, ჰასიუმი არის ელემენტი რადიოაქტიური და არასტაბილური.
ეს ნიშნავს, რომ მისი იზოტოპები აღწევს ცოტა დრო ნახევარი ცხოვრება (ატომური სახეობის მასის განახევრებისთვის საჭირო დრო). ამჟამად ცნობილია ჰასიუმის შვიდი იზოტოპი, რომელთა მასა მერყეობს 264 სთ-დან 270 სთ-მდე. მათ შორის ყველაზე სტაბილურია იზოტოპი 269Hs, ნახევარგამოყოფის პერიოდით 14 წამი.
მიუხედავად იმისა, რომ ხანმოკლე ნახევარგამოყოფის პერიოდი ართულებს ტრანსაქტინიდების ქიმიური თვისებების შესწავლას, ჰასიუმს ამ მხრივ ცოტა მეტი იღბალი ჰქონდა. 2001 წლის ივნისში გამოცხადდა, რომ ის გახდა ყველაზე მძიმე ელემენტი, რომელსაც აქვს მისი თვისებების გაანალიზება.
გერმანიის ქალაქ დარმსტადიოში ჯგუფმა მოახერხა დაახლოებით ექვსი Hs ატომის გამომუშავება, ნახევარგამოყოფის პერიოდით დაახლოებით 10 წამი. მიუხედავად იმისა, რომ ცოტა ჩანს, ეს საკმარისი იყო იმის დასადასტურებლად, რომ ჰასიუმის ოქსიდი, HsO4, აქვს ძლიერი მსგავსება მე-8 ჯგუფის მსუბუქი ელემენტების ოქსიდებთან, RuO4 და OsO4, ანუ რუთენიუმი ეს არის ოსმიუმი.
იხილეთ ასევე: Seaborgium - კიდევ ერთი სინთეზური ქიმიური ელემენტი რადიოაქტიური თვისებებით და ხანმოკლე ნახევარგამოყოფის პერიოდით
ჰასიუმის მიღება
ტრანსაქტინიდებს საერთო აქვთ წარმოების სირთულე. ზოგადად, საჭიროა უახლესი ტექნიკის, მაგ ნაწილაკების ამაჩქარებლები. მათში იონური სახეობები ეჯახება მაღალი ელემენტებს ატომური მასა ზემძიმე ელემენტების ჩამოყალიბება (რომელშიც შედის Hs).
ჰასიუმის შემთხვევაში, კვლევები, რომლებმაც დაადასტურა მისი პოზიცია პერიოდული ცხრილის მე-8 ჯგუფში, მოიცავდა მის წარმოებას მაგნიუმ-26-ის დაბომბვით, კურიუმ-248-ით, როგორც სამიზნე.
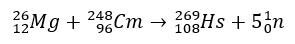
ამ ელემენტებთან დაკავშირებული ექსპერიმენტები ძვირია და, შესაბამისად, ჩვეულებრივია თეორიული კვლევების ჩატარება, სწორედ ქიმიური თვისებების გამოთვლასა და პროგნოზირებისთვის. ხანმოკლე ნახევარგამოყოფის პერიოდი კიდევ ერთი გართულებული ფაქტორია.
ექსპერიმენტული ტექნიკა გამოყოფა და გამოვლენა უნდა იყოს ძალიან სწრაფი სანდო შედეგების მისაღებად. საბოლოოდ, ამ ელემენტების რეაქციის ეფექტურობა ძალიან დაბალია, რამდენიმე ატომის ერთეულის ფარგლებშია.
სიფრთხილის ზომები ჰასიუმთან
Hs არ არის წარმოებული დიდი მასშტაბით და, შესაბამისად, მისი მანიპულირება არ შეიცავს რისკებს. გარდა ამისა, იგი მიიღება კვლევით ცენტრებში მაღალი კონტროლირებადი გარემოში.
ჰასიუმის ისტორია

ტრანსაქტინიდები იყვნენ მეცნიერული კამათის გმირები იმის გამო Ცივი ომი, ა ტრანსფერების ომი, სახელი შემუშავებული დავების მითითებით, რომლებიც მოიცავდა ფერმიუმის შემდეგ ელემენტების წარმოებას და აღიარებას (Fm, Z = 100). ამ რბოლაში ჩართული იყვნენ ლაბორატორიები:
ბირთვული კვლევების ერთობლივი ინსტიტუტი, ქალაქ დუბნაში, რუსეთი;
ლოურენს ბერკლის ეროვნული ლაბორატორია ბერკლიში, კალიფორნია;
Gesellschaft für Schwerionenforschung (GSI, უკეთ ითარგმნება როგორც ჰელმჰოლცის ცენტრი მძიმე იონების კვლევისთვის) დარმსტადიუმში, გერმანია.
108-ე ელემენტის შემთხვევაში ჩართული იყო GSI და Dubna ჯგუფები. თუმცა, მიუხედავად იმისა, რომ დუბნას მეცნიერებმა (იური ოგანესიანის ხელმძღვანელობით) პირველად განაცხადეს 108-ე ელემენტის არსებობაზე, გერმანულმა ჯგუფმა მიიღო დამსახურება, როგორც GSI-მ უფრო დამაჯერებელი შედეგები წარმოადგინა, მაშინ როცა ერთ ექსპერიმენტში მან მოახერხა 265 იზოტოპის სამი ატომის გამომუშავება, მეორეში კი 264 იზოტოპის ერთი ატომი.
ეს იზოტოპები წარმოიქმნა უნივერსალური ხაზოვანი ამაჩქარებლის გამოყენებით (Unilac, უკეთ ითარგმნება როგორც უნივერსალური ხაზოვანი ამაჩქარებელი), დაბომბვით. 208Pb მიერ 58რწმენა. 1997 წელს სუფთა და გამოყენებითი ქიმიის საერთაშორისო კავშირმა (IUPAC) აღიარა ელემენტი 108, სიმბოლო Hs, როგორც ჰასიუმი გერმანიის შტატის ჰესეს საპატივცემულოდ.
ჰასიუმზე ამოხსნილი სავარჯიშოები
კითხვა 1
ჰასიუმი, სიმბოლო Hs, ითვლება ყველაზე მძიმე ელემენტად, რომელსაც აქვს მისი თვისებები ექსპერიმენტულად შესწავლილი. იმ დროს მკვლევარებმა შეძლეს ჰასიუმის ტეტროქსიდის, HsO-ს თვისებების დადგენა4. ამ სახეობაში Hs-ს აქვს იგივე NOx, რაც მისი ჯგუფის მსუბუქ ელემენტებს, ოსმიუმს (Os) და რუთენიუმს (Ru). ჰასიუმის ტეტროქსიდში H-ების დაჟანგვის რაოდენობა უდრის:
ა) 0
ბ) +2
გ) +4
დ) +6
ე) +8
რეზოლუცია:
ალტერნატივა ე
THE ჟანგბადი, როცა ა ოქსიდი, იძენს მუხტს -2-ის ტოლი. ასე რომ, NOx H-ების, რომელსაც ჩვენ x-ს დავარქმევთ, შეიძლება გამოითვალოს შემდეგნაირად:
x + 4(-2) = 0
x - 8 = 0
x = +8
კითხვა 2
ჰასიუმის ყველაზე სტაბილური იზოტოპის, Hs, ნახევარგამოყოფის პერიოდი მხოლოდ 14 წამია. Ეს ნიშნავს:
ა) 14 წამში Hs-ის იზოტოპის მასა გაორმაგდება.
ბ) 14 წამის შემდეგ, Hs იზოტოპის მასა იქნება საწყისი მასის ნახევარზე ნაკლები.
გ) სულ რაღაც წუთში, Hs იზოტოპის მასა იქნება მისი საწყისი მასის 1/16.
დ) ერთ წუთში Hs იზოტოპის მასა იქნება მისი საწყისი მასის ზუსტად ნახევარი.
ე) 14 წამში Hs იზოტოპის მასა გაიყოფა 4-ზე.
რეზოლუცია:
ალტერნატივა C
ნახევარგამოყოფის პერიოდი მიუთითებს ატომური სახეობების რაოდენობის განახევრებისთვის საჭირო დროს. ეს ნიშნავს, რომ ყოველ 14 წამში Hs-ის რაოდენობა ორჯერ მცირდება. ამ ნახევარგამოყოფის პერიოდის დაკვირვებით, ცხადია, რომ 56 წამის შემდეგ, ოთხი ნახევარგამოყოფის პერიოდი უკვე მიღწეულია, რის გამოც Hs-ის მასა გაიყოფა 2-ზე.4, რომელიც არის 16.
სტეფანო არაუხო ნოვაისის მიერ
ქიმიის მასწავლებელი
