გამხსნელი და გამხსნელი არის ერთგვაროვანი ნარევის ორი კომპონენტი, რომელსაც ქიმიური ხსნარი ეწოდება.
- გახსნილი: არის ნივთიერება, რომელიც იფანტება გამხსნელში. ეს შეესაბამება ნივთიერებას, რომელიც დაიშლება და, ზოგადად, ხსნარში უფრო მცირე რაოდენობითაა.
- გამხსნელი: არის ნივთიერება, რომელშიც იხსნება ხსნადი ნივთიერება ახალი პროდუქტის შესაქმნელად. იგი უფრო დიდი რაოდენობით წარმოიქმნება ხსნარში.
დაშლა ხსნადს (დისპერსიულ) და გამხსნელს (დისპერანტს) შორის ხდება მათ მოლეკულებს შორის ურთიერთქმედების შედეგად.
ხსნარის ამ ორ კომპონენტს შორის განსხვავება იმაშია, რომ გამხსნელი არის ნივთიერება, რომელიც იხსნება, ხოლო გამხსნელი არის ნივთიერება, რომელიც მოქმედებს დაშლაზე.
ყველაზე ცნობილი გამხსნელი არის წყალი, რომელიც ითვლება უნივერსალური გამხსნელი. ეს იმიტომ, რომ მას აქვს უნარი დაითხოვოს დიდი რაოდენობით ნივთიერებები.
ხსნადი და გამხსნელი მაგალითები
იხილეთ ქიმიური ხსნარების რამდენიმე მაგალითი და აღმოაჩინეთ თითოეული მათგანის ხსნადი და გამხსნელი:
წყალი და მარილი
- ხსნადი: სუფრის მარილი - ნატრიუმის ქლორიდი (NaCl)
- გამხსნელი: წყალი
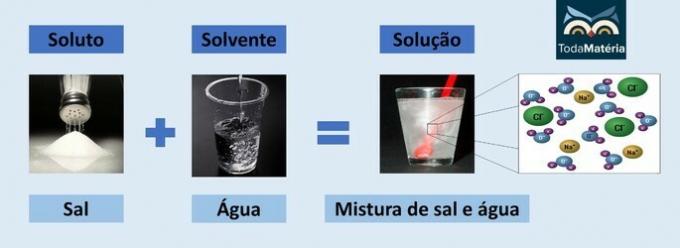
ვინაიდან ეს არის იონური ნაერთი, ნატრიუმის ქლორიდი ხსნარში ახდენს დისოცირებას და ქმნის იონებს, რომლებიც,
წყალი.წყლის დადებითი ბოძი (H+) ურთიერთქმედებს მარილის ანიონთან (Cl-) და წყლის უარყოფითი პოლუსი (O2-) ურთიერთქმედებს კატიონთან (Na+).
ეს არის ელექტროლიტური ხსნარის ტიპი, რადგან ხსნარში მყოფი იონური სახეობა ელექტროენერგიის გატარებას ახერხებს.
წყალი და შაქარი
- ხსნადი ნივთიერება: შაქარი - საქაროზა (C12ჰ22ო11)
- გამხსნელი: წყალი

შაქარი არის კოვალენტური ნაერთი და წყალში გახსნისას მოლეკულები ისინი იშლებიან, მაგრამ არ ცვლიან პირადობას.
ეს წყალხსნარი კლასიფიცირდება როგორც არაელექტროლიზური, რადგან ხსნარში დისპერსიული ხსნარი ნეიტრალურია და, შესაბამისად, არ ახდენს რეაგირებას წყალთან.
ძმარი
- ხსნადი ნივთიერება: ძმარმჟავა (CH3COOH)
- გამხსნელი: წყალი

ძმარი არის ხსნარი, რომელიც შეიცავს მინიმუმ 4% ძმარმჟავას, ა კარბოქსილის მჟავა რომელიც, როგორც პოლარული, ურთიერთქმედებს წყალთან, ასევე პოლართან, წყალბადის ობლიგაციების საშუალებით.
ხსნადობის მნიშვნელოვანი წესია, რომ მსგავსი იხსნება, როგორც. პოლარული ნაერთები იხსნება პოლარულ გამხსნელებში, ხოლო არაპოლარული ნივთიერებები იხსნება არაპოლარულ გამხსნელებში.
სხვა გადაწყვეტილებები
თხევადი ხსნარების გარდა, ასევე არსებობს გაზური და მყარი ხსნარები.
ჰაერი, რომელსაც ჩვენ ვსუნთქავთ, არის გაზური ხსნარის მაგალითი, რომლის გაზები უფრო მეტი რაოდენობით არის აზოტი (78%) და ჟანგბადი (21%).
საათზე ლითონის შენადნობები ისინი მყარი გადაწყვეტილებებია. მაგალითად, თითბერი (თუთია და სპილენძი) არის ნარევი, რომელსაც მუსიკალური ინსტრუმენტების დასამზადებლად იყენებენ.
გსურთ მიიღოთ მეტი ცოდნა? წაიკითხეთ ეს სხვა ტექსტები:
- ქიმიური გადაწყვეტილებები
- ინტერმოლეკულური ძალები
- ჰომოგენური და ჰეტეროგენული ნარევები
რა არის ხსნადობის კოეფიციენტი?
ხსნადობის კოეფიციენტი არის გახსნილი ნივთიერების ლიმიტი მოცემულ ტემპერატურაზე გამხსნელში და ქმნის გაჯერებულ ხსნარს.
ო ხსნადობის კოეფიციენტი იცვლება პირობების მიხედვით და შეიძლება გაიზარდოს ან შემცირდეს ტემპერატურისა და ხსნადი ნივთიერების ცვლილების შესაბამისად.
არსებობს ზღვარი, რომლის გამხსნელიც შეიძლება დაითხოვოს.
მაგალითი: თუ ჭიქა წყალში შაქარს ჩადებთ, პირველ მომენტში შეამჩნევთ, რომ შაქარი წყალში ქრება.
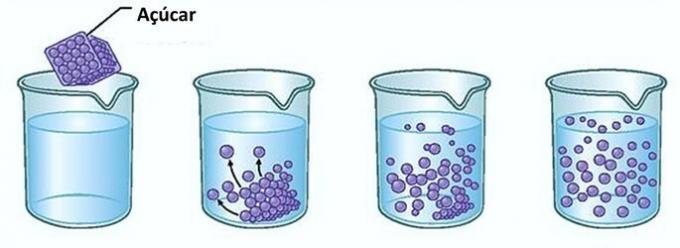
ამასთან, თუ შაქრის დამატებას გააგრძელებთ, ნახავთ, რომ რაღაც მომენტში ის დაიწყებს დაგროვებას ჭიქის ფსკერზე.
ეს იმიტომ ხდება, რომ წყალმა, რომელიც გამხსნელია, მიაღწია თავის ლიმიტს ხსნადობა და კონცენტრაციის მაქსიმალური რაოდენობა. ხსნარს, რომელიც რჩება ჭურჭლის ფსკერზე და არ იხსნება, ეწოდება ფონის სხეული.
შუშის ფსკერზე ჭარბი შაქარი არ იხსნება და გავლენას არ მოახდენს ხსნარის კონცენტრაციაზე. გარდა ამისა, შუშის ფსკერზე განთავსებული შაქარი წყალს არ გახდის ტკბილს.
გადაწყვეტილებების კლასიფიკაცია
ხსნარები შეიძლება კლასიფიცირდეს გახსნილი ხსნალის ოდენობით. ამრიგად, ისინი შეიძლება იყოს სამი სახის: გაჯერებული, უჯერი და ზეჯერ გაჯერებული.
- გაჯერებული ხსნარი: ხსნარმა მიაღწია ხსნადობის კოეფიციენტის ზღვარს, ანუ არის მაქსიმალურად გახსნილი ხსნადი გამხსნელში გარკვეულ ტემპერატურაზე.
- უჯერი ხსნარი: გახსნილი ხსნალის რაოდენობამ ჯერ ვერ მიაღწია ხსნადობის კოეფიციენტს. ეს ნიშნავს, რომ შესაძლებელია უფრო მეტი ხსნარის დამატება.
- გაჯერებული ხსნარი: უფრო გახსნილი ხსნადია, ვიდრე ნორმალურ პირობებში. ამ შემთხვევაში, ისინი წარმოადგენენ ნალექს.
გადაწყვეტილებების შესახებ მეტი ინფორმაციის მისაღებად წაიკითხეთ შემდეგი ტექსტები.:
- ხსნარების განზავება
- მორალი
- მოლარეობა
- ტიტრირება
ხსნარების კონცენტრაცია
გამხსნელიდან და გამხსნელიდან შესაძლებელია გამოთვალოთ ხსნარის კონცენტრაცია.
საერთო კონცენტრაცია განისაზღვრება, როგორც ხსნარის მოცემულ მოცულობაში გახსნილი ხსნადი მასის მასა.
კონცენტრაციის გაანგარიშება ხდება შემდეგი ფორმულის გამოყენებით:
ყოფნა,
ჩკონცენტრაცია (გ / ლ);
მ: გამხსნელი მასა (g);
ვ: ხსნარის მოცულობა (L).
მაგალითი:
(Faap) გამოთვალეთ კონცენტრაცია გ / ლ, ნატრიუმის ნიტრატის წყალხსნარში, რომელიც შეიცავს 30 გრ მარილს 400 მლ ხსნარში:
რეზოლუცია:
დააკვირდით ინფორმაციას ხსნადი და გამხსნელი რაოდენობით. 400 მლ წყალხსნარში (გამხსნელი) არის 30 გრ მარილი (ხსნადი ნივთიერება).
თუმცა, მოცულობა არის მლნ და ჩვენ უნდა გადავიყვანოთ L- ზე:
ახლა, კონცენტრაციის ცოდნისთვის, უბრალოდ უნდა გამოიყენოთ ფორმულა:
ამ შედეგით მივედით იმ დასკვნამდე, რომ როდესაც 30 გრ მარილს შეურიებთ 400 მლ წყალს, მივიღებთ ხსნარს 75 გ / ლ კონცენტრაციით.
დამატებითი ინფორმაციისთვის, თუ როგორ გამოვთვალოთ საერთო კონცენტრაცია, ეს ტექსტები გამოგადგებათ.:
- ხსნარის კონცენტრაცია
- სავარჯიშოები საერთო კონცენტრაციაზე

