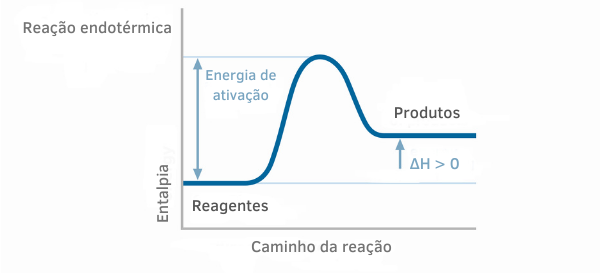
დუღილი არის თხევადიდან აირისებურ მდგომარეობამდე გადასვლა. ეს ხდება მაშინ, როდესაც მოცემული წნევის ქვეშ მყოფი სითხის ნაწილი იღებს სითბოს და აღწევს გარკვეულ ტემპერატურას.
სითბოს რაოდენობა, რომელიც სხეულმა უნდა მიიღოს, რომ მთლიანად გადაიქცეს ორთქლად, დამოკიდებულია მის შემადგენელ ნივთიერებაზე.
თხევად მდგომარეობაში მყოფ ნივთიერებას არ აქვს განსაზღვრული ფორმა, ვთქვათ, თუ მასში შედის კონტეინერის ფორმა.
პრაქტიკულად გაუგებარია, ეს წარმოადგენს შეკრულ ძალას მის შემადგენელ ნაწილაკებს შორის.
გაზურ მდგომარეობაში გადასასვლელად, ნივთიერებამ უნდა მიიღოს სითბო. ენერგიის ეს ზრდა გახდის მოლეკულების ვიბრაციას უფრო დიდი ინტენსივობით, გაზრდის მათ შორის მანძილს.
ამ გზით, შეკრული ძალა პრაქტიკულად არ არსებობს. ამ მდგომარეობაში არსებულ სხეულს არ აქვს გარკვეული ფორმა და მოცულობა.
გეიზერები არის დუღილის მაგალითები, რომლებიც ხდება ვულკანურ რეგიონებში მდებარე მიწისქვეშა წყლებთან. მაგმა აცხელებს წყალს და როდესაც ის გარკვეულ ტემპერატურას მიაღწევს, იგი იწყებს მდგომარეობის შეცვლას.
ორთქლი უფრო მეტ მოცულობას იკავებს, ზრდის ზეწოლას მიწისქვეშა ღრუში. შედეგად, ორთქლისა და სითხის ნარევი მცირე ბზარების საშუალებით გამოიდევნება ზედაპირზე.

დუღილის მახასიათებლები
თხევადი boils შემდეგ ნიმუში:
- წნევის მუდმივი შენარჩუნება, ტემპერატურა დუღილის პროცესში მუდმივი დარჩება.
- სითხის რაოდენობა მასის ერთეულზე, რომელიც საჭიროა სითხის მთლიანად ორთქლად გადაქცევისთვის, ეწოდება ორთქლის ფარული სითბოს. მისი მნიშვნელობა დამოკიდებულია ნივთიერებაზე, რომელიც ქმნის თხევადს.
- ტემპერატურა, სადაც თითოეული ნივთიერება დუღს კარგად არის განსაზღვრული და მას დუღილის წერტილს უწოდებენ.
რჩევა: როდესაც ჩვენ საჭმელს ვამზადებთ, კარგი იქნება სითბო დაბლა ჩართოთ, როდესაც წყალი ადუღდება. იმის გამო, რომ ტემპერატურა მუდმივი რჩება დუღილის პროცესში, მოხარშვის დრო იგივე იქნება მაღალი სიცხე ან დაბალი სითბო. ამ გზით, ჩვენ დაზოგავთ გაზს და გარემო მადლიერია.
ლატენტური სითბოს რაოდენობა
სითბოს რაოდენობა, რომელიც თხევადმა უნდა მიიღოს, რომ ორთქლად გადაიქცეს, დამოკიდებულია ორთქლის ფარული სითბოს და მისი მასის ღირებულებაზე.
ქვემოთ წარმოგიდგენთ ზოგიერთი ნივთიერების აორთქლების ფარული სითბოს მნიშვნელობას:

ფორმულა
სითხის სითხის საჭირო რაოდენობის გამოსათვლელად, ჩვენ ვიყენებთ შემდეგ ფორმულას:
სად,
Qვსითბოს რაოდენობა (ცაცხვი)
მ: მასა (გ)
ლვ: ორთქლის ფარული სითბო (cal / g)
მაგალითი:
რამდენი სითბოა საჭირო 100 გრ ეთანოლის ადუღებისთვის და მთლიანად ორთქლად გადაქცევისთვის?
Qვ = 100. 204 = 204 000 კალ
დუღილის ტემპერატურა
ტემპერატურა, რომელზედაც განიცდის სხეულს, დამოკიდებულია ნივთიერებაზე, რომელიც მას ქმნის და წნევაზე, რომელსაც განიცდის.
ნივთიერებების დუღილის წერტილი განისაზღვრება ლაბორატორიაში. მაგალითად, წყლის დუღილის წერტილი, რომელიც 1 ატმოსფეროს განიცდის, არის 100 ° C. რკინა არის 2800 ° C, ხოლო წყალბადის არის - 252,8 ° C.
სხვა ნივთიერებების ფაზის ცვლილების ტემპერატურის ცოდნისთვის ასევე წაიკითხეთ დუღილის წერტილი.
რაც უფრო მცირე წნევას განიცდის სხეული, მით უფრო დაბალია მისი დუღილის წერტილი. ეს ნიშნავს, რომ დიდ სიმაღლეზე მყოფ ქალაქებში საჭმლის მომზადებას გაცილებით მეტი დრო სჭირდება.
საჭმლის უფრო სწრაფად მოსამზადებლად ვიყენებთ წნევის გაზქურებს. გაზქურის ეს ტიპი იყენებს დალუქვის სისტემას, რომლის წყალობითაც ზეწოლა უფრო მეტია ვიდრე ატმოსფერული წნევა.
უფრო მაღალი წნევა ადუღების წერტილს უფრო მაღალს ხდის. წყლის შემთხვევაში ის დუღდება ტემპერატურაზე, რომელსაც შეუძლია მიაღწიოს 120 ºC, რაც ამცირებს ხარშვის დროს.
ფაზის ცვლილებები
თხევადიდან გაზურ მდგომარეობაში გადასვლას ზოგადად უწოდებენ აორთქლებაროგორც იგი მოიცავს, ადუღების გარდა, კიდევ ორ პროცესს: აორთქლება და გათბობა.
აორთქლება ხდება თანდათან, საჭირო არ არის კონკრეტული ტემპერატურის მიღწევა. მეორეს მხრივ, გათბობა ხდება მაშინ, როდესაც თხევადს ვათავსებთ ზედაპირზე, რომელიც დუღილის წერტილზე მაღლა ტემპერატურაზეა.
ჯერ კიდევ არსებობს სახელმწიფოს შეცვლის სხვა პროცესები. ისინი არიან:
- შერწყმა
- გამყარება
- გათხევადება ან კონდენსაცია
- სუბლიმაცია
ქვემოთ მოცემულ დიაგრამაზე ჩვენ წარმოვადგენთ ამ სამს მატერიის ფიზიკური მდგომარეობა და შესაბამისი სახელმწიფო ცვლილებები:
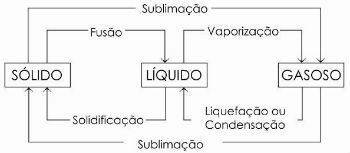
მეტი რომ გაიგოთ, წაიკითხეთ ასევე წყლის ფიზიკური მდგომარეობა.
Სავარჯიშოები
Enem - 1999 წ
ტექსტი უნდა იქნას გამოყენებული შემდეგი ორი კითხვისთვის.
წნევის გაზქურის საშუალებით საჭმლის მომზადება წყალში ბევრად უფრო სწრაფად ხდება, ვიდრე ჩვეულებრივი გაზქურის. მის სახურავს აქვს რეზინის დალუქვა, რომელიც არ უშვებს ორთქლს, გარდა ცენტრალური ხვრელისა, რომელზეც წონა აკონტროლებს წნევას. გამოყენებისას, მაღალი წნევა გროვდება შიგნით. მისი უსაფრთხო მუშაობისთვის აუცილებელია ცენტრალური ხვრელის სისუფთავის დაცვა და უსაფრთხოების სარქვლის არსებობა, რომელიც ჩვეულებრივ მდებარეობს საფარში.
ქვემოთ მოცემულია წნევის გაზქურის სქემა და წყლის ფაზის დიაგრამა.
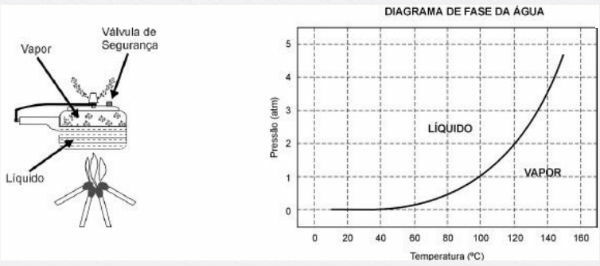
1) წნევის გაზქურის გამოყენების უპირატესობა არის საჭმლის მომზადების სიჩქარე და ეს გამოწვეულია
ა) ზეწოლა მის შიგნით, რომელიც ტოლია წნევის გარეთ.
ბ) მისი ინტერიერის ტემპერატურა, რომელიც აღემატება წყლის წყლის დუღილის ტემპერატურას.
გ) დამატებითი სითბოს რაოდენობა, რომელიც გადადის ტაფაზე.
დ) სარქველით გამოყოფილი ორთქლის რაოდენობა.
ე) მისი კედლის სისქე, რომელიც უფრო მეტია, ვიდრე ჩვეულებრივი ტაფები.
ალტერნატივა ბ: მისი შინაგან ტემპერატურაზე, რომელიც აღემატება წყლის დუღილის ტემპერატურას ადგილზე.
2) თუ ეკონომიკისთვის, ჩვენ შევამცირებთ სითბოს წნევის გაზქურის ქვეშ, როგორც კი ორთქლი გამოვა სარქველიდან, რათა უბრალოდ შევინარჩუნოთ დუღილის დრო, ხარშვის დრო
ა) უფრო დიდი იქნება, რადგან ტაფა "გაცივდება".
ბ) იქნება უფრო მცირე, რადგან ამცირებს წყლის დაკარგვას.
გ) მეტი იქნება წნევის შემცირებისთანავე.
დ) უფრო მეტი იქნება, ვიდრე აორთქლება შემცირდება.
ე) არ შეიცვლება, რადგან ტემპერატურა არ იცვლება.
ალტერნატივა e: არ შეიცვლება, რადგან ტემპერატურა არ იცვლება.