ო ატომური სხივი ელემენტები არის პერიოდული თვისება, რომელიც განსაზღვრავს ატომის რადიუსს, რომელიც იცვლება პერიოდულ ცხრილში ელემენტის პოზიციიდან.
ამრიგად, მათ შეუძლიათ გაიზარდონ და შემცირდნენ ატომური ნომერი (Z) ელემენტისა, რომელიც შეესაბამება ატომების ბირთვში არსებული პროტონების რაოდენობას.
შეჯამება, ატომური რადიუსი შეესაბამება ორი მეზობელი ატომის ბირთვებს შორის მანძილს ნახევრად, რაც გამოიხატება შემდეგნაირად:
r = დ / 2
საიდან:
რ = რადიუსი
დ = ბირთვული მანძილი
ზოგადად, ატომური რადიუსი იზომება პიკომეტრებში (საათში), მრიცხველის ქვე-ნამრავლი (1 პიკომეტრი = 10-12 მ.). გაითვალისწინეთ, რომ როდესაც მითითება არ არის ატომი, არამედ იონი, ნაპოვნი რადიუსი არის იონური რადიუსი.
ატომური რადიუსის ვარიაცია
პერიოდულ ცხრილში ატომური რადიუსის ზრდა ჩანს შემდეგ სურათზე:
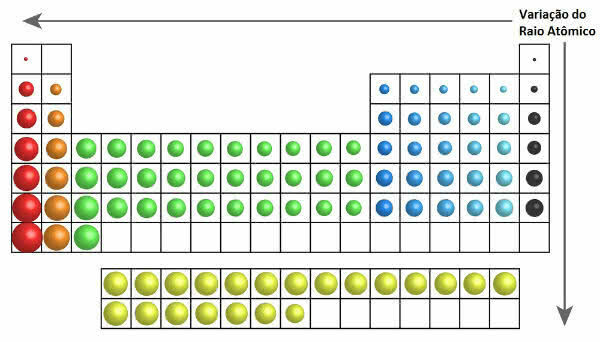 ატომური რადიუსის ვარიაცია პერიოდულ ცხრილში
ატომური რადიუსის ვარიაცია პერიოდულ ცხრილში
ამრიგად, ვერტიკალურად (ოჯახები ან ჯგუფები) ატომური რადიუსი იზრდება ზემოდან ქვემოთ. ჰორიზონტალურზე (პერიოდებზე), ისინი იზრდება მარცხნიდან მარჯვნივ.
იხილეთ შებრუნებული ვარიაცია ელექტრონული Affinity და ელექტრონეგატიურობა.
იონიზაციის ენერგია
იონიზაციის ენერგია (ან პოტენციალი) ეს ასევე არის პერიოდული თვისება, რომელიც განსაზღვრავს ენერგიას ელექტრონის გადასაადგილებლად, რაც გამოიხატება ელექტრონულ ვოლტებში (eV).
წაიკითხეთ ასევე: პერიოდული თვისებები.
შეამოწმეთ მისაღები გამოცდის შეკითხვები კომენტარებით: სავარჯიშოები პერიოდულ ცხრილზე.
