მოლეკულა არის იგივე ან განსხვავებული ელემენტების ატომების ჯგუფი. იხილეთ რამდენიმე მაგალითი:
ჰ2ო - ორი განსხვავებული ელემენტისგან წარმოქმნილი მოლეკულა (ორი წყალბადის ატომი და ერთი ჟანგბადის ატომი);
კლ2- მოლეკულა, რომელიც წარმოიქმნება მხოლოდ ერთი ქიმიური ელემენტისგან (ქლორის ორი ატომი).
საათზე მოლეკულები შეიძლება კლასიფიცირდეს პოლარული ან აპოლარული:
არაპოლარული: მოლეკულები, რომლებსაც არ აქვთ პოლუსები (დადებითი და უარყოფითი);
პოლარული: მოლეკულები, რომლებსაც აქვთ პოლუსები (დადებითი და უარყოფითი).
ამ ტექსტში ჩვენ ხაზს გავუსვამთ პოლარული მოლეკულები. იდენტიფიცირება პოლარული მოლეკულა, ქვემოთ მოცემული სტრატეგიის გამოყენება შეგვიძლია:
) იონური ნაერთი (იონური ბმით წარმოქმნილი)
თუ ნივთიერება წარმოიშვა იონური ბმა (ლითონსა და არამეტალს შორის), ეს ნიშნავს, რომ იგი იონების (კატიონისა და ანიონის) მიერ წარმოიქმნება. ამიტომ, ეს ნივთიერება ავტომატურად წარმოადგენს პოლარული მოლეკულები, ვინაიდან იონებს აქვთ დადებითი და უარყოფითი მუხტები.
მაგალითები:
NaCl (Na არის ლითონი, და Cl არის არამეტალი);
CaO (Ca არის მეტალი, ხოლო O არის არამეტალი);
MgS (მგ არის მეტალი, ხოლო S არის არამეტალი).
ბ) მოლეკულური ნაერთები (ჩამოყალიბდა კოვალენტური ბმით)
როდესაც ნაერთი მოლეკულურია, თითოეული შემთხვევა უნდა გავაანალიზოთ, რადგან რამდენიმე სხვადასხვა მოლეკულის შესაძლებლობა გვაქვს. ქვემოთ მოცემულია რამდენიმე მაგალითი და წესი, რომლებიც დაგეხმარებათ პოლარული მოლეკულური ნაერთების განსაზღვრაში:
- დიატომიური მოლეკულა სხვადასხვა ელემენტებით
თუ მოლეკულური ნაერთი მხოლოდ ორი ატომისგან შედგება და ეს ორი ატომი სხვადასხვა ელემენტისგან არის, ავტომატურად მოლეკულა იქნება პოლარული, რადგან ორ ატომს აქვს განსხვავებული ელექტრონეგატიურობა. მაგალითები: HBr და NO.
- მოლეკულები ორი ან მეტი ატომით (იგივე ან განსხვავებული)
მოლეკულებში, რომელთა ატომების რაოდენობა ორზე მეტია, უნდა გავითვალისწინოთ ღრუბლების რაოდენობა ლიგანდები და არა-შემკვრელები, რომლებიც იმყოფებიან მოლეკულის ცენტრალურ ატომში და შეადარეთ იგი ატომზე დამაგრებული თანაბარი ატომების რაოდენობას. მთავარი. სავალდებულო ღრუბლები არის ერთი ბმა (თითოეული ატომის ვალენტური გარსიდან ერთი ელექტრონი), ორმაგი ბმა (ორი ელექტრონები თითოეული ატომის ვალენტური გარსიდან) ან სამმაგი (სამი ელექტრონი თითოეული ატომის ვალენტური გარსიდან) ჩართული). არა სავალდებულო ღრუბლები არის ვალენტური გარსის ელექტრონების წყვილი, რომლებიც არ მონაწილეობენ ობლიგაციებში.
ნუ გაჩერდები ახლა... რეკლამის შემდეგ მეტია;)
დაკვირვება: იცოდეთ ელექტრონების რაოდენობა მოცემული ატომის ვალენტურ გარსში, იცოდეთ მხოლოდ მისი პერიოდული ოჯახი:

იმის დასადგენად, არის თუ არა მოლეკულა პოლარული, საკმარისია შეამოწმოთ, განსხვავდება თუ არა ცენტრალურ ატომში არსებული ღრუბლების რაოდენობა მასზე თანასწორი ატომების რაოდენობისგან. იხილეთ რამდენიმე მაგალითი:
HCN
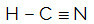
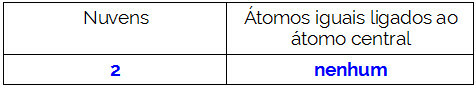
მოლეკულის ცენტრალური ატომი ნახშირბადია და აქვს ორი განსხვავებული შემკვრელის,ორი სავალდებულო ღრუბელი (ერთჯერადი და სამმაგი) და არასასურველი ელექტრონების წყვილი (ეს არის VIA ოჯახიდან, მას აქვს ოთხი ელექტრონი ვალენსიის გარსში და იყენებს ოთხივეს, ერთს ერთ შეერთებაში და სამს სამში). ამ მიზეზით, იგი ქმნის პოლარულ მოლეკულას.
მოკლედ:
NH3
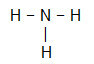
მოლეკულის ცენტრალური ატომი არის აზოტი და აქვს სამი თანაბარი ლიგანი და საერთო ჯამში ოთხი ღრუბელი, სამი სავალდებულო ღრუბელი (სამი ერთი ობლიგაცია) და ერთი არაბმული (ეს არის VA ოჯახიდან, მას აქვს ხუთი ელექტრონი) ვალენტობის ფენაში და იყენებს მხოლოდ სამს, თითო თითოეულ შეერთებაში, ორი ტოვებს არა შემკვრელები).
ამის გამო, NH ცენტრალური ატომი3 ქმნის პოლარულ მოლეკულას.
Მოკლედ:

CH2ო
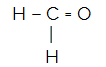
მოლეკულის ცენტრალური ატომი ნახშირბადია და აქვს ორი ერთნაირი და ერთი განსხვავებული ლიგანი, ასევესამი სავალდებულო ღრუბელი (ორი ერთი და ერთი ორმაგი ობლიგაცია), წყვილი არ არის შემაკავშირებელი ელექტრონი (ეს არის VIA ოჯახიდან, მას აქვს ოთხი ელექტრონი ვალენტურ გარსში და იყენებს 4-ს, ორი სინგლში და ორს წყვილი). ამის გამო, იგი ქმნის პოლარულ მოლეკულას.
მოკლედ:
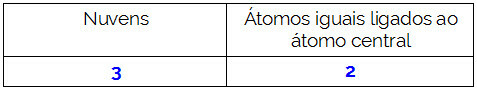
ჩემ მიერ. დიოგო ლოპეს დიასი
გსურთ მიუთითოთ ეს ტექსტი სასკოლო ან აკადემიურ ნაშრომში? შეხედე:
DAYS, დიოგო ლოპესი. "პოლარული მოლეკულები"; ბრაზილიის სკოლა. Ხელმისაწვდომია: https://brasilescola.uol.com.br/quimica/moleculas-polares.htm. წვდომა 2021 წლის 28 ივნისს.
იონური ნაერთები, იონური ნაერთების ძირითადი მახასიათებლები, იონებს შორის კავშირი, ელექტრონების საბოლოო გადაცემა, ელექტროსტატიკური მოზიდვის ძალები იონებს, უარყოფით და დადებით იონებს, ანიონებს, კათიონებს, იონურ კავშირს, მოლეკულურ სტრუქტურას შორის ის
Ქიმია
მოლეკულური ნივთიერებები, დუღილის ტემპერატურა, საკონტაქტო ზედაპირი, დუღილის წერტილი, მოლეკულური მიზიდულობის ძალები, ქიმიური ბმა, მოლეკულური ნაერთები, კოვალენტური ქიმიური ბმები, იონური ბმები, მეტალის ბმები, ფიზიკური მდგომარეობები ცუდი