1 緩衝液 これは、強酸または強塩基が添加されたときに培地のpHまたはpOHが変化するのを防ぐために使用される混合物です。
緩衝液には2つのタイプがあります。
1. 弱酸とその共役塩基の混合物;
2. 弱塩基とその共役酸の混合物。
それぞれの例と、少量の強酸または強塩基を培地に加えたときにどのように機能するかを見てみましょう。
1. 弱酸とその共役塩基の混合物:
このような溶液を形成するために、弱酸は酸と同じ陰イオンの塩と混合されます。
たとえば、酢酸(H3CCOOH(ここに))および酢酸ナトリウム(H3CCOONa(s)). 両方にアセテートアニオンがあることを確認してください:(H3CCOO-(ここに)). これらのイオンの濃度は、実際には大きな塩の解離によるものです。 酸イオン化は小さい。

ここで、次の追加の可能性で何が起こるかに注意してください。
- 少量の強酸の添加:
強酸を加えると、ヒドロニウムイオンHの濃度が高くなります。3O+1、酢酸は弱酸であるため、酢酸陰イオンはプロトン(H+)ヒドロニウム。 このようにして、それらは反応し、より多くの酢酸が形成されます:

その結果、培地のpHは実質的に変化しません。 しかし、強酸をどんどん加えると、酢酸陰イオンがすべて消費されて緩衝効果がなくなる時が来ます。
- 少量の強塩基の追加:
強塩基の添加はOHイオンの濃度を増加させます-. しかし、これらのイオンはHイオンによって中和されます3O+1 酢酸のイオン化で放出される:

この反応により、Hイオンの濃度3O+1(ここに) が減少し、平衡が酸イオン化の増加に向かってシフトするため、溶液のpH変動は非常に小さくなります。 Hイオンの濃度3O+1(ここに) それは実質的に一定になります。
今やめないで... 広告の後にもっとあります;)
この場合、バッファの容量にも制限があります。 したがって、塩基をどんどん追加すると、酸のイオン化のバランスは、すべての酸が消費されるまで、そのイオン化に向かってますますシフトします。
2. 弱塩基とその共役酸の混合物:
このタイプの緩衝液は、弱塩基と、塩基と同じ陽イオンを含む塩溶液で構成されています。
たとえば、水酸化マグネシウム、MgOHによって形成された緩衝液を考えてみましょう。2(aq) (弱塩基)および塩化マグネシウム、MgCl2(s) (塩)。 両方ともカチオンマグネシウム(Mg2+(ここに)). 塩基の解離が弱いため、媒体に存在するマグネシウムイオンは事実上すべて塩の解離に由来します。
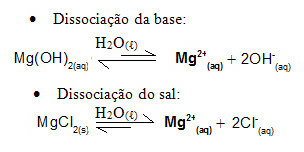
- 少量の強酸の添加:
この場合、Hイオン3O+1 強酸の添加により、OHイオンによって中和されます-、弱塩基解離に由来します。 これにより、基本解離バランスが右にシフトします。
したがって、OHイオンの濃度が高いため、pHの変動(存在する場合)は非常に小さくなります。- 一定のまま。 塩基全体が解離すると、緩衝効果はなくなります。
- 少量の強塩基の追加:
加えられた強塩基は解離を受けてOHイオンを放出します-. 水酸化マグネシウムは弱塩基であるため、塩から解離して放出されるマグネシウムは、OHと反応する傾向が大きくなります。-:

したがって、OHイオンの増加- Mg(OH)の比例増加によって相殺されます2(aq). その結果、pHは大きな変化を受けません。
この効果は、すべてのマグネシウムカチオンが消費されたときに終了します。
ジェニファー・フォガサ
化学を卒業
学校や学業でこのテキストを参照しますか? 見てください:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "緩衝液とは何ですか?"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/o-que-uma-solucao-tampao.htm. 2021年6月28日にアクセス。
化学

あなたの知識をテストし、化学物質のバランスに関する解決された演習のこのリストで詳細を学びましょう。 この資料を通じて、平衡定数(Kp、Kc、Ki)、平衡シフト、pH、pOH、およびいわゆる緩衝液での平衡の操作方法をよりよく理解できるようになります。
溶液、固溶体。 液体溶液、気体溶液、気体と液体によって形成された溶液、液体によって形成された溶液。


