と呼ばれる イオンビーム イオンのサイズ。 この特性の研究は、原子半径とイオンに関する知識に依存しています。
原子半径: は中性原子のサイズ(原子核から最後の電球までの理論上の距離)の尺度です。
イオン:電子を失う(陽イオン)または得る原子(陰イオン)。
原子核内の陽子 原子 エレクトロスフィアに存在する電子(負の粒子)に引力を及ぼします。 陽子の数が多いほど、この引力は大きくなり、逆もまた同様です。 原子内の電子の数がこれらの粒子の損失または増加によって変更されると、陽子と電子の間の引力は次のように変更されます。
陽イオンの場合:
エレクトロスフィア内の電子の数は、原子核内の陽子の数よりも少なくなります。 これにより、原子核の引力が大きくなり、電子が原子核に近づきます。 エレクトロスフィア。 その結果、原子の半径が小さくなります。 したがって、陽イオンの半径は常にその中性原子の半径よりも小さくなります。
中性原子半径>陽イオン半径
陰イオンの場合:
エレクトロスフィア内の電子の数は、原子核内の陽子の数よりも多くなります。 この場合、原子核によって加えられる引力は、エレクトロスフィアに存在する電子間の反発力によって打ち負かされ、その結果、原子の半径が大きくなります。 したがって、陰イオンの半径は常にその中性原子の半径よりも大きくなります。
今やめないで... 広告の後にもっとあります;)
陰イオン半径>中性原子半径
以下に示す2つの状況は、イオンの半径に何が起こるかを示す良い例です。
1番目)中性ナトリウム原子(11Na)およびナトリウムカチオン(11で+)
中性ナトリウム原子には11個の陽子(黄色の球)と11個の電子(赤い球)がありますが、ナトリウムカチオンには11個の陽子と10個の電子があります。

ナトリウム中性原子モデル
中性ナトリウム原子が電子を失うと、半径は小さくなります。
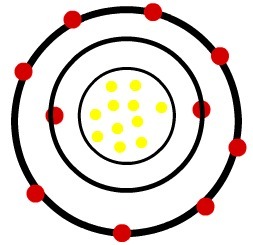
ナトリウムカチオンのモデル
観察: 3番目のレベルは、それが持っていた唯一の電子を失ったため、空になり、したがって無視されたため、陽イオンの画像には表示されませんでしたが、存在しています。
2番目)リン中性原子(15P)およびリンカチオン(15P-3)
中性のリン原子には15個の陽子(黄色の球)と15個の電子(赤い球)がありますが、リンの陰イオンには15個の陽子と18個の電子があります。
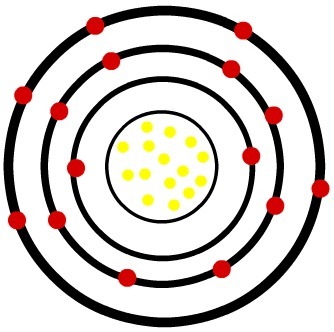
中性リン光原子のモデル
中性のリン原子が3つの電子を獲得すると、半径が大きくなります。
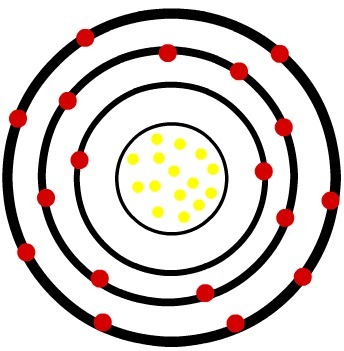
リン光物質の陰イオンのモデル
私によって。DiogoLopesDias
学校や学業でこのテキストを参照しますか? 見てください:
DAYS、ディオゴロペス。 "イオン半径"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/raio-ionico.htm. 2021年6月28日にアクセス。


