反応の動的平衡または化学平衡は、順方向と逆方向の反応が同時に発生したときに発生します。 これらのいわゆる可逆システムは、両方向の矢印で表されます。  または
または  . 上の画像では、ヨウ素ガスと水素ガスの間の可逆反応の例が引用されています。
. 上の画像では、ヨウ素ガスと水素ガスの間の可逆反応の例が引用されています。
反応の開始時に、反応物の量は最大であり、生成物の量はゼロです。 しかしながら、反応物は互いに反応し、それらの濃度を減少させ、形成された生成物の濃度を増加させる。 直接反応の発生率も低下しています。
生成物の濃度が増加すると、逆反応が始まり、反応物が再び形成されます。 逆反応の発生率も増加します。
一定の温度で化学平衡に達すると、順方向反応と逆方向反応の発生速度は等しくなります。
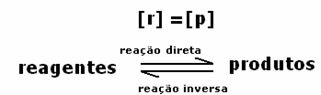
すべて直接 =すべて 逆
率は同じですが、濃度は異なります。 試薬と生成物の濃度が同じになる可能性は低いです。 まれなケースでのみ、これが発生します。 ほとんどの場合、試薬の濃度は製品の濃度よりも高くなり、その逆も同様です。
したがって、の開発率をグラフィカルに表す3つの可能な方法があります。 直接および逆反応、反応物および生成物の濃度を 時間。 それぞれのケースを見てみましょう:
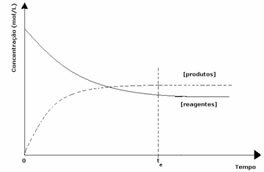
1番目のケース: 等しい濃度:
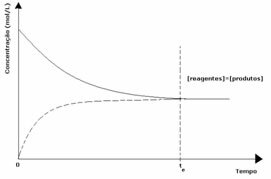
グラフに見られるように、時間tでそして 順方向反応と逆方向反応は同じです。この場合、反応物と生成物の濃度は同じです。 したがって、バランスはどちらの側にもシフトせず、以下に示すように、両方の反応の強度は同じです。
今やめないで... 広告の後にもっとあります;)
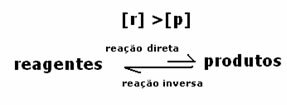
2番目のケース: 製品の濃度よりも高い試薬の濃度:
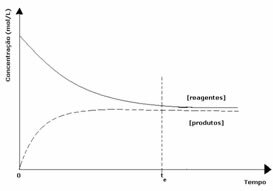
この場合、平衡に達すると、反応物の濃度が生成物の濃度よりも高くなることが観察されます。 したがって、より多くの反応物が存在する場合、逆反応がより強い強度で起こっていると結論付けられる。 反応は左にシフトします:
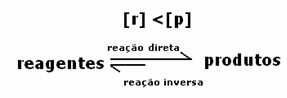
3番目のケース: 試薬よりも高い生成物の濃度:
平衡状態では生成物の濃度が高いため、これは反応が 直接反応(生成物の形成を伴う)がより大きく発生するため、右にシフト 強度。
反応が右に向かうか左に向かうかを示すのは、温度のみに依存する平衡定数Kです。
ジェニファー・フォガサ
化学を卒業
ブラジルの学校チーム
学校や学業でこのテキストを参照しますか? 見てください:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "化学バランスのグラフィック研究"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/estudo-grafico-equilibrio-quimico.htm. 2021年6月28日にアクセス。
化学

あなたの知識をテストし、化学物質のバランスに関する解決された演習のこのリストで詳細を学びましょう。 この資料を通じて、平衡定数(Kp、Kc、Ki)、平衡シフト、pH、pOH、およびいわゆる緩衝液での平衡の操作方法をよりよく理解できるようになります。