物質の特性は、他の要因の中でもとりわけ、分子が極性または非極性であるという事実によって決定されるため、分子の極性は非常に重要な側面です。
分子の極性の決定は、 双極子モーメント または 結果として生じる双極子モーメント、その記号は 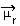 . 分子内の各結合の双極子モーメントについて話している場合、記号はギリシャ文字のmi(µ)です。
. 分子内の各結合の双極子モーメントについて話している場合、記号はギリシャ文字のmi(µ)です。

双極子モーメントがゼロに等しい場合、分子は非極性になりますが、非ゼロの場合、それは極性であることを意味します。

この結果として生じる双極子モーメントを決定する際に考慮すべき2つの重要なことがあります。 それらが何であるかを見てみましょう:
1) 電気陰性度の違い 反応に関与する元素の原子間。 たとえば、HF分子は電気陰性度に著しい違いがあります。これは、フッ素が水素よりもはるかに多く、結合内の電子対を引き付けるためです。 したがって、電荷の分布は対称的ではなく、電気双極子があります。
この双極子は、最も多くの電子を集中させる端に面するベクトル、つまり、最も電気陰性度の低い原子から最も電気陰性度の高い原子までで表されます。 したがって、この場合、以下に示すように、唯一のベクトルが結果のベクトルになります。
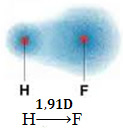
ベクトル値は、デバイ単位(D = 3.33)で与えられる双極子モーメントと同じであることに注意してください。 10-30 クーロン。 地下鉄)。 双極子モーメントがゼロではないため、分子と結合は次のようになります。 極地.
今やめないで... 広告の後にもっとあります;)
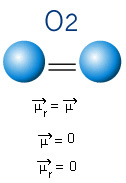
下の分子にも原子が2つしかない分子がありますが、この場合は単体に相当し、1種類の元素だけで構成されています。 したがって、電気陰性度の違いはありません。 原子はまた、対称的に分布している電子を引き付けます。 結果として生じる双極子モーメントはゼロに等しいので、結合と分子の両方が 無極性.
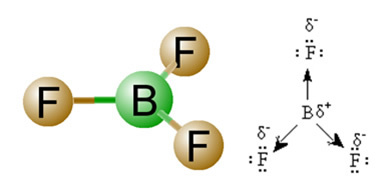
2) 分子幾何学、つまり、ベクトルの空間配置。 BF分子3 それは3つの極性結合を持っており、フッ素が最も電気陰性度が高いため、ベクトルがそれに向けられています。 ただし、原子の空間配置は三角形のフラットであるため、これにより電子は中心原子の周りに対称的な分布を持ちます。 したがって、結果として、これら3つのベクトルは互いに打ち消し合い、双極子モーメントはゼロに等しくなります。 したがって、BF分子3 é アポレート.
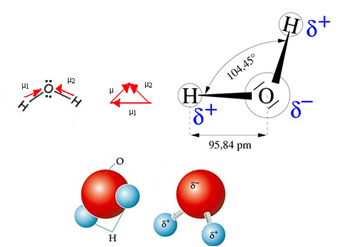
水分子には2つのベクトルがありますが、その空間ジオメトリはフラットではなく、V字型になっています。 次の図では、このようにベクトルが互いに打ち消し合わないため、電子は非対称に分布し、最も電気陰性度の高い原子である酸素にさらに集中していることに注意してください。 したがって、双極子モーメントはゼロとは異なり、水分子は 極地:
ジェニファー・フォガサ
化学を卒業


