熱力学の第1法則によれば、どの熱力学プロセスでも熱量は Q システムが受け取る仕事は、システムが行う仕事に内部エネルギーの変動を加えたものに等しくなります。
圧力が一定の場合、システムが外部媒体と交換する熱は、作業と内部エネルギーの変更に使用されます。 多くの実際の状況では、化学反応の場合のように、システムは大気圧にさらされます。 上の図は、このタイプのプロセスのPV図を示しています。
この場合、第一法則の方程式では、
Q =τ+ ∆U
いずれの項もゼロではありません。 作業は、次のように、ボリューム変動volumeVの関数として記述されます。
τ= P.∆V
理想的な単原子ガスの特定のケースでは、エネルギーは次のように書くことができます。

したがって、熱力学の第1法則をΔVの関数として書くことができます。


媒体と交換される熱は(5/2)P.ΔVであり、全体の40%(P.ΔVに相当)が作業の実行に使用されます。 (3/2)P.ΔVは全体の60%に相当し、内部エネルギーを変化させるために使用されます。 この結果は、理想的な単原子ガスに対して有効です。
熱は(理想気体の法則を使用して)温度変化に次のように関係しています。
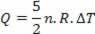
したがって、供給される熱は、温度の変化または体積の変化によって計算できます。
ドミティアーノ・マルケス
物理学を卒業
ソース: ブラジルの学校- https://brasilescola.uol.com.br/fisica/primeira-lei-para-processos-isobaricos.htm
