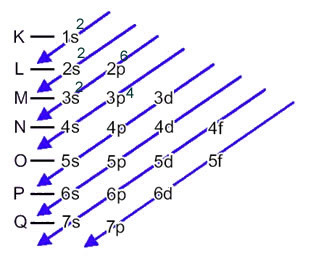
中性または基本状態の原子の電子の電子分布は、通常、 ポーリング図, 下に示された:
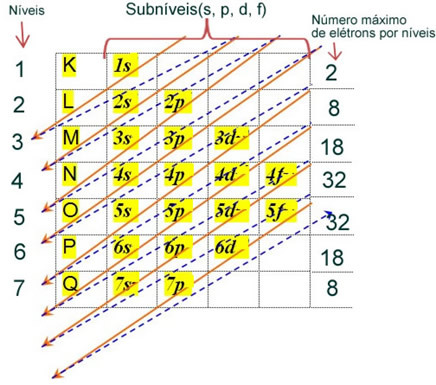
この配布の詳細なルールは、当社のWebサイトの次の2つのテキストに記載されています。電子の電子分布「と」電子配布ルール”.
イオンの電子分布は、最初は中性状態の原子の場合と同じように機能します。 違いは1つだけです。 イオンは電子を獲得または喪失した原子であるため、これを考慮して次のことを行う必要があります。

重要な観察事項は次のとおりです。 変更は最もエネルギッシュなサブレベルではなく、最も外側のサブレベルで行われます。
イオンが カチオン、 我々はしなければならない 電子を取り除く 彼が失ったこと。 例を見てみましょう:
鉄原子(原子番号= 26)は、エネルギー順にサブレベルで次の電子分布を持っています。 1秒2 2秒2 2p6 3秒2 3p6 4秒2 3D6. 電子層に関しては、次のものがあります。 K =2; L = 8; M = 14; N = 2。
この分布は、以下のポーリング図に示されています。
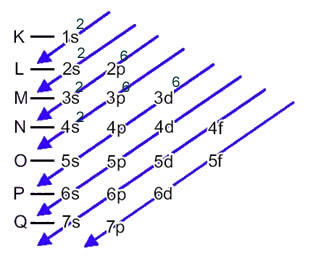
鉄原子が2つの電子を失うと、Feカチオンに変わります。2+. だから、あなたの電子配布をするとき、私たちはしなければなりません 最後のシェルから2つの電子を削除します(N)そして最もエネルギッシュなサブレベルからではなく、 以下に示すように:
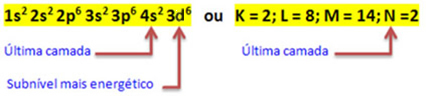
したがって、Feカチオンの電子的分布2+ によって与えられます:
1秒2 2秒2 2p6 3秒2 3p6 3D6 または K = 2; L = 8; M = 14
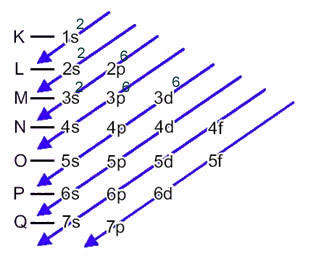
さて、私たちがの電子配布を実行する必要がある場合 アニオン、 我々はしなければならない 受け取った電子を追加します.次の例で、これがどのように行われるかを確認してください。
硫黄陰イオン(16s2-)は硫黄原子から形成されます(16S)電荷2-で示されるように、2つの電子のゲインによって。 その基底状態の電子分布は次の式で与えられます。
1秒2 2秒2 2p6 3秒2 3p4 または K = 2; L = 8; M = 6
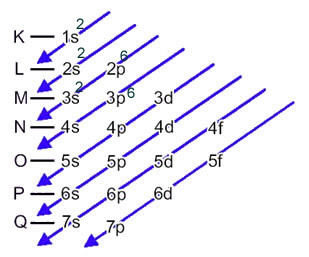
この場合、最後のサブレベルはエネルギーサブレベル3pと同じです。 したがって、硫黄アニオンの2つの電子をそれに追加します。
1秒2 2秒2 2p6 3秒2 3p6 または K = 2; L = 8; M = 8
ジェニファー・フォガサ
化学を卒業
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/distribuicao-eletronica-ions.htm


