木を燃やしても溶けない理由を理解するために、まず溶けた物質とは何か、つまり液体の状態にあることを思い出してみましょう。
固体、液体、気体の状態の違いは、粒子の凝集状態だけです。 3つの状態では、物質は同じ粒子で構成されていますが、それらの間には多かれ少なかれスペースがあります。
固体状態では、粒子は互いに接近しており、移動の自由度はあまりありません。 液体状態では、粒子はより自由に動き、動くことができます。
木材の多く(50%)は、実際にはポリマーであるセルロースから作られていることがわかりました。 ポリマーは、モノマーと呼ばれるいくつかの分子の結合によって形成されます。 セルロースの場合、以下に示すように、数百のβ-グルコース分子の結合によって形成されます。 セルロースは次の式を持ちます(C6H10O5)番号 そして400,000uのオーダーの分子量に達します。
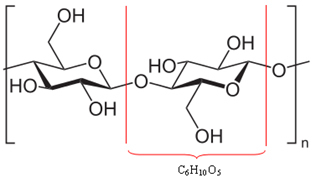
それらは巨大な分子であるため、木材を構成するこれらのポリマーは簡単に動くことができません。 また、セルロースを構成するβ-グルコース分子にはヒドロキシル基(─OH)があることに注意してください。 これらの基は水素を互いに結合します。これは最も強いタイプの分子間力であり、ポリマーをしっかりと結合します。

セルロースポリマーを構成する分子間の水素結合*
したがって、 これらの結合を断ち切るには、システムに非常に多くのエネルギーを投入して、木材が溶ける前に分解して、もはや木材ではなくなるようにする必要があります。
したがって、燃やされると、木材は化学反応を起こします。これは、物理的な状態の単なる変化以上のものです。 その分子は最終的に分解され、空気中に存在する酸素と再結合し、炭素ガスや水などの新しい物質を形成します。

* ソース と画像の作者: laghi.l.
ジェニファー・フォガサ
化学を卒業
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/por-que-madeira-nao-derrete.htm

