一部の化合物は、安定性を実現するために価電子シェルに8つの電子を持つ必要がないため、オクテット則の例外と見なされます。 いくつかの要素が最後のシェルに電子のオクテットを持つ義務を免れる理由を今すぐ学びましょう。
ベリリウム (Be)
オクテット則の例外は、2つの単結合を持つ化合物を形成できるため、価電子シェル内の4つの電子だけで安定化するためです。 
水素(H)は結合を作るために2つの電子をあきらめる必要があるので(H-まあ-H)、ベリリウム(Be)原子はその電子を共有し、安定性を実現します。
アルミニウム (Al)
価電子シェル内の6つの電子で安定性を実現するため、オクテット則の例外です。 アルミニウム原子はその電子を提供する傾向があるため、他の原子と3つの単結合を形成できます。 
この場合、アルミニウム(Al)は3つのフッ素(F)原子と3つの結合を形成しました。
ボロン (B)
それは3つの単結合を持つ分子物質を形成します。 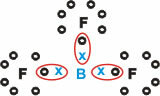
ホウ素(B)は、その電子をフッ素(F)原子に供与する傾向があることに注意してください。フッ素(F)原子は、オクテット則に従い、価電子シェルに8つの電子を必要とします。 ホウ素が電子を放出すると、フッ素は形成されたオクテットで安定します。
リリア・アルベス
化学を卒業
ブラジルの学校チーム
続きを見る!
オクテット理論
一般化学 - 化学 - ブラジルの学校
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/excecoes-regra-octeto.htm
