(電子を共有することによって)共有結合を実行する化合物の物理的および化学的特性の分析は、これらの材料の間に大きな違いがあることを示しています。 しかし、これらの特性自体を見る前に、分子物質と共有結合物質の違いを見てみましょう。
で 分子物質 それらは、原子が共有結合を介して結合し、決定された数の分子を生成するときに形成されるものです。
ただし、共有結合は、非常に多くの不確定な数の原子を持つネットワーク構造の化合物を生成することもあります。 高分子. そのような物質は呼ばれます 共有化合物 または 共有ネットワークソリッド. これらの化合物の例としては、ダイヤモンド(C)、グラファイト(C)、二酸化ケイ素(SiO)があります。2)および炭化ケイ素(SiC)。
それでは、その主なプロパティを見てみましょう。
- 室温での物理的状態: 周囲条件下では、分子化合物と共有結合化合物が見つかります 3つの物理的状態で (固体、液体、気体)。
例:
O 固体: 砂糖(ショ糖)、シリカ(砂)、ダイヤモンド、グラファイト;
O 液体: 水、アセトン、エタノール;
O ガス状: 硫化水素、塩素ガス、臭素ガス、水素ガス。

- 融点と沸点: 一般的に、これらの物質の融点と沸点は次のとおりです。 イオン性物質よりも小さい.
共有結合物質は分子物質よりも沸点が高く、常に1000°Cを超えます。 これは、分子がより密接に結合して結晶格子を形成するため、状態を変化させるためにより多くのエネルギーを供給する必要があるためです。
共有結合および分子化合物の沸点と融点を妨げる2つの要因:a モル質量 そしてその 分子間力.
モル質量が大きいほど、分子の慣性が大きくなり、その結果、沸点と融点が高くなります。 モル質量を概算すると、分子間力がわかります。 最も強い分子間力は水素結合の力であり、より高い沸点と融点につながります。 中間体は永久双極子であり、最も弱いものはより低い沸点と融点につながり、誘導双極子です。
- 電流: 純粋な形では、液体と固体の両方が電流を伝導しません。
例外はグラファイトです。グラファイトは、二重結合の電子が共鳴し、特定の移動度を持っているため、固体の形で電流を流します。
- 溶解性: 極は極に溶解し、非極性は非極性に溶解します。
- 粘り強さ: 共有結合物質の衝撃や機械的衝撃に対する耐性は低いです。 一般に、それらは、ケイ酸ナトリウムとケイ酸カルシウムによって形成されるガラスの場合に示されるように、もろい固体です。

- 靭性: 一般的に、それらは高い硬度を持っています。 グラファイトを除いて、その炭素原子は他の3つの炭素原子と結合しているため、一定の移動度を持つ六角形のプレートを形成し、柔らかくなります。 このため、潤滑剤としても使用されています。
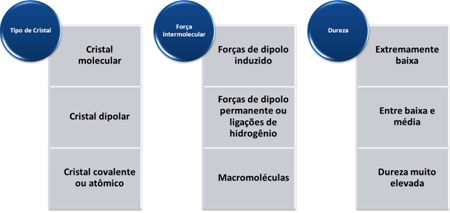
これらの物質の硬度は、下の表に示すように、結晶の種類によって異なります。
ジェニファー・フォガサ
化学を卒業
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/propriedades-dos-compostos-covalentes-moleculares.htm

