THE ニホニウム, 原子番号 113と記号Nhは、周期表の13族に属する化学元素です。 また、自然界には見られない超重元素です。 したがって、その取得は、核融合反応を介して、人工的にのみ行うことができます。 ニホニウムの化学的特性はまだそれほど明確ではありませんが、場合によっては、より軽い対応物であるタリウムと同様に動作すると推測されます。
ニホニウムは最初に溶融によって得られました 70亜鉛と 2092003年に日本の理研研究所でBi。 ロシアとアメリカの科学者も元素113の発見者として認められることを求めたが、IUPACは日本の科学者を認めた。 この名前は、日本人が母国と呼んでいる日本という言葉を指しています。
あまりにも読んでください: ガリウム—周期表の第13族に属する別の化学元素
ニホニウムについての要約
これは、第13族元素に含まれる合成化学元素です。 周期表.
その生産は2003年に日本の理研研究所で始まりました。
これは、2015年に周期表に最近含まれた元素のグループを構成します。
彼の研究はまだ非常に最近のものですが、タリウムなどのグループ13の他の元素にリンクしようとする人もいます。
その生産は 核融合、の同位体を使用して 70亜鉛と原子 209Bi。
ニホニウムの性質
シンボル: いや
原子番号: 113
原子質量: 278〜286 c.u.(Iupacによる非公式)
電子配置: [Rn]7秒2 5f14 6d10 7p1
最も安定な同位体:286Nh(9.5秒 人生の半分、6.3秒増加または2.7秒減少する可能性があります)
化学シリーズ: グループ13、超重元素
ニホニウムの特性
ニホニウム、記号Nhおよび原子番号113、 周期表に含まれる最後の要素の1つでした. その正式化は2015年12月30日に国際純正応用化学連合(IUPAC)によって行われ、その名前は2016年半ばにのみ正式に発表されました。
周期表のこの領域の元素は非常に不安定であり、自然界では見つけることができません。 したがって、存在の疑いに直面して、それらは、より大きな安定性を達成するために、ほぼ瞬時に放射性崩壊(αやβなどの核粒子の放出)を受けるでしょう。
しかし、それらが核粒子を放出すると、それらは核変換を受けることになります。つまり、それらは新しい化学元素になります。 したがって、Nhなどの超重元素は実験室で生成する必要があります。 合成化学元素.
Nhは、他の超重元素と同様に、 相対論的効果 —簡単に言えば、相対性理論のために、観察されたものから期待されたものまでの距離。 したがって、相対論的効果の結果をシミュレートする理論分野の数学的研究は、そのニホニウムを指摘しました クォーツと弱く相互作用する可能性がありますが 持つため に良い吸着 ゴールド、その軽い対応物のように、タリウム(Tl)。
予備的な理論的研究はまた、 ボラティリティ Nhから。 石英への吸着に関しては、例えばタリウムは容易にTlOHを形成し、ニホニウムも同じように疑われます。
それでも、どうやって 研究はまだ非常に予備的で最近のものです、生産されたものの多くは議論の余地があり、ニホニウムの物理化学的性質を正確に決定することは困難です。
ニホニウムの入手
要素113は、今日まで、次の2つの方法で取得されています。 常温核融合反応、亜鉛(Zn、Z = 30)とビスマス(Bi、Z = 83)の融合、および 要素115のアルファ崩壊.
最初の例では、 亜鉛 の10%に加速されます 光の速度、2つの原子核の反発力を克服するために。 次に、同位体が生成されます 279Nh、これは最終的に中性子を放出し、 278Nh。

半減期は約34ミリ秒で、同位体 278Nhは、元素メンデレビウム(Md)に対して6回のアルファ崩壊(アルファ粒子放出)を受けます。
2番目のケースでは、元素113は、合成後の元素115(現在はマスコビウムとして知られています)のアルファ崩壊から生じます。 一つの方法は、イオンの熱核融合反応です 48同位体を含むCa 243ああ、 288マクそして、アルファ崩壊によって、 284Nh、これはアルファ崩壊を受け続けます。
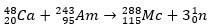
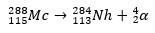
も参照してください: ハッシウム—その特性を分析するための最も重い合成化学元素
ニホニウムの歴史
要素113の検索は2003年に始まりました。 理研研究所の日本人研究者は、 70光速の10%の亜鉛と衝突する 209Bi、核融合反応による。 したがって、彼らは私たちが今知っているものを何とか作り出しました 278Nh。
しかし、それは2012年だけでした 日本の研究者は完全なアルファ崩壊系列を検出することができました 要素113の、発見を主張するためにIUPACに連絡します。
日本の努力と並行して、ユーリイ・オガネシアンが率いるロシアの科学者は、 アメリカの科学者はまた、元素のアルファ崩壊を通して元素113を特定するようになりました 115. そのような実験はまた、ロシアとアメリカの科学者を元素113の認識をめぐって争わせた。

しかし、IUPACは、理研研究所からの証拠がより堅固であると判断したため、日本人が要素113に名前を付ける権利を持つことを許可しました。 選ばれた名前は、国を参照して、nihônio、シンボルNhでした 日本. 日本という言葉は、「昇る太陽の国」を意味する2つの漢字を使用して日本人によって書かれ、日本または日本と読みます。
ニホニウムという名前も選ばれたのは、1908年に日本の化学者小川正孝が次のように発表したためです。 元素43を発見し、それを日本語と名付け、シンボルNp(今日はネプツニウムに属する、Z = 93). しかし、後に、元素43は不安定であり、自然界には見られず、1937年にのみ合成されたことが証明されました。 テクネチウム (Tc)。
このように、日本人は周期表から姿を消しました。 しかし、数年後、実際、小川は元素75(現在は レニウム). しかし、その時までに、元素レニウムはすでに1925年に公式に発見され、洗礼を受けていました。
ニホニウムに関する解決済みの演習
質問1
記号Nh、原子番号113のニホニウムは、半減期が短いため、自然界では見られない化学元素です。 それらの中で最も耐久性のある、 286Nh、約9.5秒です。 半減期は種の量が半分になるのに必要な時間であることを知って、 上記の同位体の量が量の1/16になるのに何秒かかりますか イニシャル?
A)9.5
B)19
C)28.5
D)38
E)47.5
解像度:
代替案D
9.5秒ごとに、同位体の量は半分に減少します。 したがって、9.5秒後、その量は最初の量の半分になります。 さらに9.5秒、合計19秒で、量は再び半分に減少し、最初の1/4に達します。
28.5秒で、さらに半減期が経過すると、量は再び半分に減少し、最初の量の1/8に達します。 最後に、38秒後、金額は再び半分に減少し、ステートメントで要求されているように、最初の金額の1/16に達します。 したがって、必要な時間は38秒です。
質問2
2003年、日本の理化学研究所で元素113の検索が開始されました。 当時、科学者は 278亜鉛原子とビスマス原子の核融合によるNh。
引用された同位体にはいくつの中性子が含まれていますか?
A)113
B)278
C)391
D)170
E)165
解像度:
代替案E
の数 中性子 次のように計算できます。
A = Z + n
ここで、Aは パスタ アトミック、Zは原子番号、nは中性子の数です。 値を代入すると、次のようになります。
278 = 113 + n
n = 278-113
n = 165
StefanoAraújoNovais著
化学の先生

