THE 元素の周期的分類 1913年にヘンリーモンスリー(1887-1915)によって提案されました。 元素の原子核内の陽子の数に応じた一定の間隔での特性 化学。
のために 周期性の法則、現在の周期表の元素を整理するために使用される基準は、原子番号(Z)の昇順です。
118の化学元素は、周期表のグループと期間に配置されています。 物理的および化学的性質に応じて、区別することが可能です 金属, 非金属 (非金属)および 半金属 (メタロイド)。

縦線は 18グループ テーブルと同様の化学的性質を持つ要素をまとめます。 水平線はに対応します 7期間 同じ数の電子層を持つ要素を提示します。
水素は、電子的に分布しているため、グループ1の上に位置する元素ですが、それらと共通の特徴はありません。
をチェックしてください 周期表 完全で更新されました。
金属
周期表のほとんどの化学元素は金属として分類されています。 金属の主な特徴は次のとおりです。
- 彼らは特徴的な輝きを持っています。
- それらは密度が高く、展性があり、延性があります。
- 彼らは電気と熱の良い伝導体です。
- それらは、水銀を除いて、固体状態の周囲条件下で存在します。
周期表の金属元素は次のとおりです。
アルカリ金属 (グループ1):リチウム、ナトリウム、カリウム、ルビジウム、セシウム、フランシウム。
アルカリ土類金属 (グループ2):ベリリウム、マグネシウム、カルシウム、ストロンチウム、バリウム、ラジウム。
代表事項、グループ1および2の元素に加えて、アルミニウム、ガリウム、インジウム、タリウム、ニオン、スズ、鉛、フレロビウム、ビスマス、マスコビウム、およびリバモリウムがあります。
外側の遷移金属 周期表の中央部分を占める要素は次のとおりです。
- グループ3:スカンジウムとイットリウム。
- グループ4:チタン、ジルコニウム、ハフニウム、ラザホージウム。
- グループ5:バナジウム、ニオブ、タンタル、ドブニウム。
- グループ6:クロム、モリブデン、タングステン、シーボーギウム。
- グループ7:マンガン、テクネチウム、レニウム、ボーリウム。
- グループ8:鉄、ルテニウム、オスミウム、ハッシウム。
- グループ9:コバルト、ロジウム、イリジウム、マイトネリウム。
- グループ10:ニッケル、パラジウム、プラチナ、ダルムシュタット。
- グループ11:銅、銀、金、レントゲン。
- グループ12:亜鉛、カドミウム、水銀、コペルニシウム。
内部遷移金属 グループ3の一部であり、ランタニドおよびアクチニド系列の元素に対応する元素です。
ランタニドシリーズは、ランタニウム、セリウム、プラセオジミウム、ネオジミウム、プロメチウム、サマリウム、ユーロピウム、ガドリニウム、テルビウム、ジスプロシウム、ホルミウム、エルビウム、ツリウム、イッテルビウム、ルテチウムで構成されています。
アクチニドシリーズには、アクチニウム、トリウム、プロトアクチニウム、ウラン、ネプツニウム、プルトニウム、アメリシウム、キュリウム、バークリウム、カリホルニウム、アインスタイニウム、フェルミウム、メンデレビウム、ノーベリウム、ローレンスの元素が含まれています。
についてもっと読む アルカリ金属.
非金属
非金属は周期表の右側にあり、金属とは反対の特性を持っています。たとえば、次のようになります。
- 光沢のある外観はありません。
- それらは電気と熱の良い伝導体ではないので、絶縁体として使用されます。
- それらは低い沸点と融点を持っているので、多くは液体状態で自然界に見られます。
君は 非金属元素 周期表には、水素、窒素、酸素、炭素、リン、セレン、硫黄、ハロゲン、希ガスが含まれます。
君は ハロゲン グループ17に属する元素は、フッ素、塩素、臭素、ヨウ素、アスタチン、テネシン、および希ガスファミリーです。
君は 希ガス グループ18に属する元素は、ヘリウム、ネオン、アルゴン、クリプトン、キセノン、ラドン、オガネソンです。
詳細については、 希ガス そしてその ハロゲン.
半金属
半金属または半金属は、ホウ素、シリコン、ゲルマニウム、ヒ素、アンチモン、テルル、ポロニウムです。 これらの元素は、金属と非金属の中間の特性を持っています。
また、 周期表ファミリー.
代表的な要素と遷移要素
要素を分類する別の方法は、要素を代表的な要素と遷移要素に分割することです。 原子の電子分布.
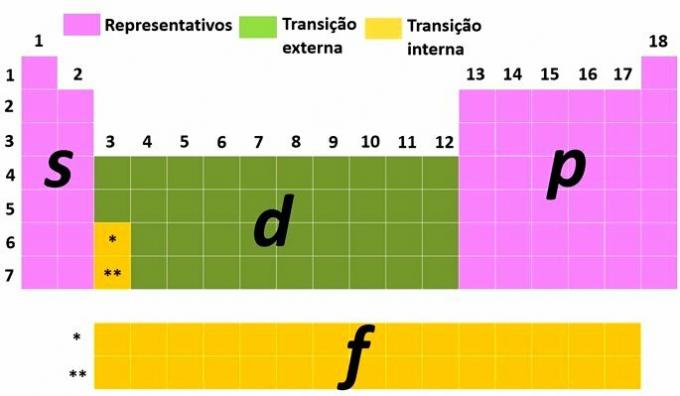
君は 代表的な要素 で最もエネルギッシュなサブレベルで終わる電子配置を持つものです s (グループ1および2)または ために (グループ13、14、15、16、17および18)。

君は 遷移元素 に分けられます 外部遷移、サブレベルで最もエネルギーの高い電子を持つ元素 d とのそれら 内部遷移、最もエネルギーの高い電子はサブレベルにあります f.

内容についてより多くの知識を得る:
- 周期表
- 周期表の練習
- 周期表の構成に関する演習



