THE フランシウム、記号Fr、原子番号87は、のグループ1に属する元素です。 周期表、アルカリ金属。 しかし、グループの他の元素とは異なり、フランシウムには安定同位体がなく、発見さえ困難でした。 実際、フランシウムは 発見される最後の要素 天然サンプルで分離されました。
その大きな原子の不安定性は、目に見える重いサンプルを取得することを可能にしないため、その物理化学的特性は他のアルカリ金属のデータから推定されます。 地球の地殻にはフランシウムが30グラムしかないと推定されており、 地球上で2番目に希少な元素、アスタチンのみの後ろ。
あまりにも読んでください: ルビジウム—特殊なガラスや原子時計の製造に使用される元素
フランシウムの概要
フランシウムは周期表の第7周期にあるアルカリ金属で、記号Fr、Z = 87です。
安定同位体がなく、地球上で2番目に希少な元素です。
その最も安定な同位体は 人生の半分 22分。
それは最大の要素です 原子線 最も電気陽性であることに加えて、周期表の。
それは核プロセスによってのみ得ることができ、分離するのは困難です。
フランシウムに関連する実用的なアプリケーションはまだありません。
フランシウムの特性
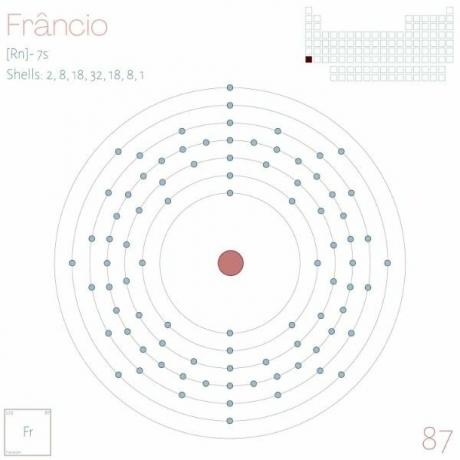
シンボル:神父
原子質量:223.02u。
融点:22°C(推定)。
沸点: 665°C(推定)。
密度:2.5g /cm³(推定)。
電気陰性度: 0,79.
エレクトロニックディストリビューション:[Rn] 7s1.
→ 化学元素の周期的および非周期的特性に関するビデオレッスン
フランシウムの特徴
フランシウム いくつかの同位体があります、しかし同位体233が最も安定しており、半減期は22分に達します。 同位体212だけが21分の同様の半減期を持っていますが、他のものはそれに近づくことさえなく、数秒のオーダーの半減期を持っているかもしれません。

このすべて 原子の不安定性 重要な物理的特性と特性の決定を妨げます。 実際、既知の特性は極端な条件下で得られました。 希釈 (10のオーダーの濃度-15 mol / L)。
アルカリ金属として、その酸化数は+1であることが知られています。 実験はまたそのフランシウムを示した 最も要素です 電気陽性 周期表の. この元素が表にあるもう1つの主要な位置は、直径が最大で2.7オングストローム(10-10 m)。
他のアルカリ金属と同様に、フランシウムは溶液中に残りますが、他の元素は水酸化物、炭酸塩、フッ化物、硫化物、クロム酸塩などの形で沈殿します。
あまりにも読んでください: 放射性元素とは何ですか?
フランシウムの入手
Frの最も安定な同位体であるフランシウム223は アクチン-227のアルファ放射によって最初に検出されました. 衝撃によりフランシウム(同位体212)を生成することも可能です ゴールド (197Au)酸素18(18O)原子炉内。
フランシウムはいくつかの方法で入手できます。 例えば、 でそれを沈殿させる可能性があります セシウム、 終えた 塩 過塩素酸塩(ClO)などの難溶性元素4-)、ヘキサクロロ白金酸塩(PtCl62-)、ヨウ素酸塩(IO4-)、他の人の間。 ただし、セシウムとフランシウムの分離は非常に難しいと予想されます。
1960年代と1970年代に開発された他の方法では、 セシウムおよびルビジウム溶液からのフランシウムの分離 陽イオン交換樹脂を介して。 アクチニウム-227のアルファ放出から発見されたフランシウム-223は、選択的沈殿技術によってアクチニウムおよび他の分解生成物から分離することもできます。 比較的成功して使用されている別の手法もあります。約300°Cの温度での塩化フランシウム(FrCl)の昇華です。
フランシウムの用途
ラットを用いた試験では、フランシウムが腎臓、肝臓、唾液腺に蓄積すると結論付けられました。 さらに、それを核医学、癌の診断に適用する試みがありましたが、それを準備して分離することが困難であったため、プロジェクトは実行不可能でした。 この特性は、その低い半減期に加えて、フランシウムを作ります 数少ないものの1つ 要素 実用的なアプリケーションはありません.
しかし、持っているという事実 周期表の最大原子半径 に電子が1つしかない 原子価層 それは何人かの研究者にその性質について好奇心をそそらせます。 2002年、米国の研究者グループは、元素について詳しく知るために30万個のフランシウム原子をトラップすることに成功しました。
私たちのポッドキャストをチェックしてください: ダイヤモンドのように硬い:それはどういう意味ですか?
フランシウムの歴史
フランシウムの歴史の中で際立っているのは、人々がフランシウムを発見したと言った回数です メンデレーエフは1871年にこの元素の存在を予測しています、 名義で eka-セシウム.
元素83、ビスマスの後、周期表には、ウランやトリウムなどの例外を除いて、放射性で不安定な元素のみが表示されることが長い間知られています。 それでも、これは多くの科学者が自然源で要素87を探すことを思いとどまらせず、多くの場合、その発見を主張しています。

例えば、 1925年に、ロシアの化学者Dobroserdovは弱いを観察しました 放射能 のサンプルで カリウム、これは要素87であると結論付け、名前を付けます russium、彼の母国に敬意を表して。 しかし、その事実の最も良い説明は、実際には、同位体からの放射能が検出されたということでした。 40K、天然カリウムの約0.012%を構成するベータエミッター。
1926年、英国の化学者Druce and Loringは、硫酸マンガン(II)のスペクトル線を分析すると、 彼らはまた、要素87に関連するいくつかの行を観察すると推定しました。 の名前 アルカリニウム. しかし、証拠の弱さは研究者が前進することを思いとどまらせました。
その後、1930年に、フレッドアリソンは、ポルサイト(セシウムに富む鉱石)とリチア雲母( リチウム その構成で)。 アリソンは名前を提案しました 処女 米国バージニア州に敬意を表して。 しかし、1934年に、マクファーソンはアリソンの発見に不正確さを示しました。
2年後、アインシュタインのブラウン運動の理論を確認したことで知られるフランスの物理学者、ジャン・ペランは、 したがって、原子の存在の十分な証拠は、光線を使った一連の実験でローマの物理学者ホリア・フルベイに加わった バツ。 次に、要素87の期待される結果を取得し、すぐに名前を付けました。 モルダビウム、モルドバ地域に関連して、フルベイの発祥の地。 しかし、再び、その解釈に照らして作品は批判されました。
研究者の誰も理解できませんでしたが、何が起こったのかというと、フランシウムは非常に不安定な同位体を持ち、半減期が非常に短いということです。 不幸はそのようなものでした 要素87の存在さえ考慮されました.
しかし、1939年に、元素87の発見は、他ならぬ実験助手として始めた誰かによって起こりました。 マリー・キュリー、 パリで: ザ フランスのマルグリット ペリー. 放射性サンプルの取り扱いと精製に関する優れた専門知識を備えたペリーは、アクチニウムの放射性サンプルである元素89の分析を任されました。
科学者 アクチニウムによって生成されたアルファおよびベータ放出を最初に観察した、21分の半減期を持つ新しい要素を明らかにします。 その後、フランス人女性は慎重に発見を発表し、1946年に博士論文を擁護しました。 要素87:アクチニウム-K.
その後、新しい要素は、最初はFaのシンボルで、母国に敬意を表してフランシウムと名付けられました。 1949年、 国際純正応用化学連合(Iupac)は、ペリーによって与えられた名前で元素を確認しました、しかし1951年にシンボルを神父に変更しました。
フランシウムに関する解決済みの演習
質問1
フランシウム(Fr、Z = 87)は、半減期が短く不安定なアルカリ金属です。 しかし、他のアルカリ金属と同様のいくつかの特性を持っていることが知られています。
上記の情報に基づいて、フランシウムと臭素の間で形成される可能性のある化合物は何ですか(Br、Z = 35)?
A)FrBr2
B)神父2br
C)FrBr
D)FrBr3
返事
アルカリ金属としてのフランシウムのNOXは+1です。 すでに臭素、 ハロゲン、酸素がない場合、NOXは-1に等しくなります。 したがって、それらの中で最も可能性の高い化合物は文字C、FrBrです。
質問2
原子半径は、原子のサイズを区別するだけでなく、原子の反応性やその他の特性を理解するのに役立つため、非常に重要な周期特性です。
周期表の元素の中で、原子半径が最大の元素は次のとおりです。
A)F
B)Cs
C)H
D)神父
E)Og
返事
元素の周期が大きいほど原子半径が大きくなり、 電子 原子価層で。 したがって、最大の半径を持つ元素は、周期表の7番目の周期にあり、価電子が1つしかないため、フランシウムFrです。
StéfanoAraújoNovais著
化学の先生