本文に記載されているように「化学反応式」、化学反応を表し、それらが処理される方法、それらの定量的および定性的側面を理解するために、化学反応式を使用することが合意されました。 化学反応式には、存在する物質とそれらが反応する適切な比率を示す記号と数字が含まれています。
これらの方程式を解釈することにより、化学量論計算の実行に役立つ重要なデータを見つけることができます。 ただし、最初のステップでは、方程式のバランスをとる必要があります。つまり、反応物の原子の総数が生成物の原子の総数と等しくなければなりません。 このバランシングを実行する方法は、「」というテキストで理解できます。方程式のバランス”.
ただし、この場合、用語の意味など、いくつかの重要な概念を理解する前に、次のことを行ってください。 指数、化学量論係数およびモル. これらの用語について以下で説明し、反応の定量的部分をよりよく垣間見ることができます。
- 索引: は、化学式に存在する各元素の原子数を示す数です。 この番号は問題の要素の右側にあり、下付き文字、つまり小さいフォントサイズで表示されます。
例:
NS2O (水物質の化学式)
どういう意味ですか:
- この物質を構成する元素は、H(水素)とO(酸素)です。
- 各元素のインデックスは、水分子の式にそれぞれの原子がいくつ存在するかを示します。
NS2O→ O-index:酸素原子は1つだけです。
↓
H指数:水素原子が2つあることを示します。
酸素の場合、書かれた数字がないことに注意してください。これは、上で説明したように、その元素の原子が1つしかないことを意味します。
現在、数式に括弧が表示される場合があります。 これをどのように解釈すればよいですか? 以下の例を参照してください。
ここ3(ほこり4)2(リン酸カルシウム物質の化学式)
- Ca含有量は、化学式にカルシウム元素の3つの原子が存在することを示しています。
- P(リン)とO(酸素)は括弧内にあるため、外側のインデックス(この場合は2)は両方に属します。 したがって、式にそれぞれの原子がいくつあるかを調べるには、それらのインデックスに外側のインデックスを個別に乗算する必要があります。 これがどのように行われるかに注意してください。

今やめないで... 広告の後にもっとあります;)
P→インデックス1O→インデックス4
P = 1。 2 O = 4。 2
P = 2 O = 8
つまり、2つのリンと8つの酸素原子があります。
- 化学量論係数: は、各物質の量と反応に関与する分子の割合を示す式の前にある数字です。 したがって、インデックスの場合のように、係数が1に等しい場合、暗黙的に示されているように、それを書き留める必要はありません。
例:
2NS2 + 1O2 → 2 NS2O(この水生成反応は導入図に示されています)
↓ ↓ ↓
反応係数
この式では、係数を通じて、2分子の水素ガスが1つの酸素ガスと反応して、2分子の水を生成物として形成することが示されています。 したがって、この反応の化学量論比は2:1:2です。
反応中に存在する各元素の原子の総数を見つけるには、係数に各元素のインデックスを掛ける必要があります。
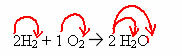
試薬:
H = 2。 2 = 4個の水素原子
O = 1。 2 = 2個の酸素原子
製品:
H = 2。 2 = 4個の水素原子
O = 1。 2 = 2個の酸素原子
反応物と生成物に同じ量を与えたことに注意してください。これは、反応が正しくバランスされていることを意味します。
- モル(物質量):化学反応式では、係数はモルの量または物質の量を示すと見なされます。 したがって、前のケースでは、2モルのHがあります2 1molのOと反応する2、生成物として2モルのHを生成2O。
ジェニファー・フォガサ
化学を卒業
学校や学業でこのテキストを参照しますか? 見て:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "化学反応式の量的項"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/termos-quantitativos-uma-equacao-quimica.htm. 2021年7月27日にアクセス。


